
英语原文共 8 页,剩余内容已隐藏,支付完成后下载完整资料
硫氰酸根离子作选择性助剂提高Ag/TiO2光催化制氢性能
Yeoseon Choi, Hyoung-il Kim, Gun-hee Moon, Seongwon Jo, and Wonyong Choi*
大韩民国,浦航科技大学化学工程与工程学院,Pohang 790-784。
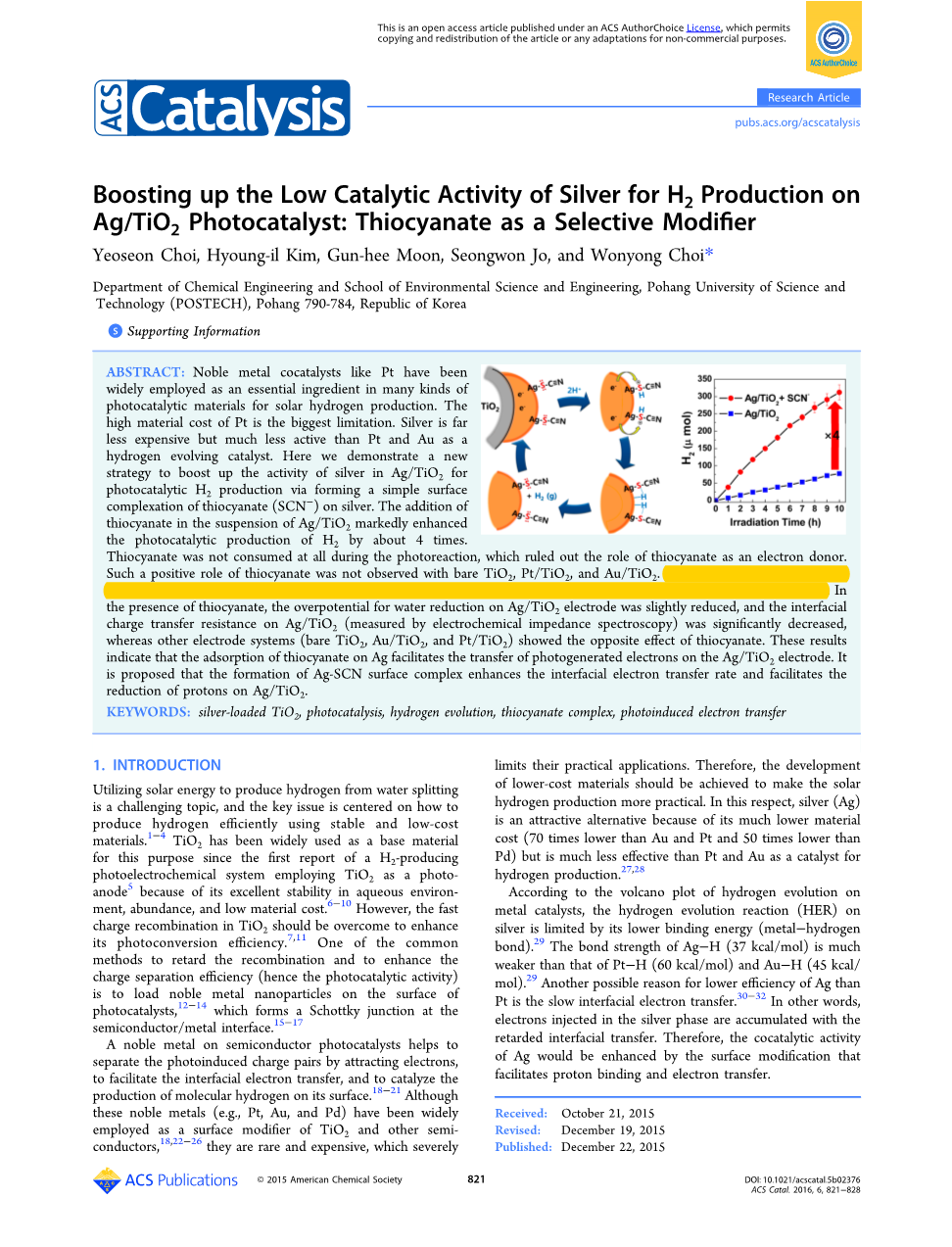
摘要:贵金属助剂,如铂,已经被广泛应用到各种光催化制氢材料中。但铂金属的成本较高限制了其作为光催化助剂的发展。同样作为析氢助剂的银比铂和金成本低,但也存在着活性较低的问题。本文提出了一种通过在银表面复合SCN-来提高光催化剂Ag/TiO2中银的活性的方法。光催化制氢测试结果表明,相比于Ag/TiO2,络合SCN-的Ag/TiO2光催化剂光催化制氢效率提高4倍左右。此外,硫氰酸根离子在反应过程中没有被消耗,这就排除了硫氰酸根离子作为给电子体的作用。同时在纯TiO2、Pt/TiO2和Au/TiO2中,硫氰酸根离子的作用不明显。通过拉曼光谱和EDS对硫氰酸根离子在银上的选择性化学吸附的测试,表明在硫氰酸根离子存在下,Ag/TiO2电极上的开路电势略有降低,电化学阻抗法测试Ag/TiO2的界面电荷转移电阻明显降低,而其它电极体系,如纯TiO2、Au/TiO2和Pt/TiO2,则与Ag/TiO2的趋势相反。结果表明,硫氰酸根离子吸附在Ag上促进光生电子在Ag/TiO2上的转移,Ag-SCN表面配合物的形成提高了Ag/TiO2界面电子传递速率,促进了质子的还原。
关键词:Ag/TiO2,光催化,析氢,硫氰酸根离子配合物,光诱导电子转移
1.引言
利用光解水制氢是一个具有挑战性的课题,课题的关键是如何利于稳定、低成本的材料有效的产氢。自第一次报道光催化制氢采用TiO2材料,TiO2由于其优越的水环境稳定性、丰富度和低成本,使其成为广泛应用的光催化材料。但是,要进一步提升TiO2光催化效率,就必须克服空穴电子的快速复合。负载贵金属在光催化剂表面组成Schottky结在半导体或金属表面是阻碍空穴-电子对快速复合和提高电荷分离效率的常用方法之一。
在半导体表面的贵金属通过吸引电子分离光生电子对,促进界面电子转移,催化表面氢气的产生。尽管贵金属,例如,Pt、Au和Pd,作为表面修饰剂已经被广泛应用到TiO2和其他半导体材料上,但他们产量小并且成本高的特点严重的限制贵金属的实际应用。因此,开发一种低成本的材料使光催化制氢更加符合实际是当务之急。在这方面,由于其极低的价格Ag是一个具有吸引力的代替品(比Au和Pt低70倍,比Pd低50倍),但是Ag的产氢效率要比Pt和Au低的多。
根据金属催化剂上的氢反应的火山图。,银较低的键能限制了它的析氢反应,Ag-H(37 kcal/mol)的键强度远远弱于Pt-H(60 kcal/mol)和Au-H(45 kcal/mol)的键的强度。Ag低效率的另一个可能原因是电子转移速率远低于Pt,注入银的电子因为缓慢的界面转移而积累。因此,表面修饰促进质子结合和电子转移能够使Ag复合催化剂催化性能的提高。
银表面对于硫复合物有很强的吸引力,硫氰酸根离子是一种类卤化物阴离子,具有很强的负电性很容易吸引银离子。在此我们报道了负载了硫氰酸根离子的Ag/TiO2光催化制氢性能有很大的提升,且在此光化学反应过程硫氰根离子的表面没有发生任何化学转化,而对于Pt/TiO2和Au/TiO2硫氰酸根离子没有这样的正面效应。硫氰酸根离子在银上形成了表面复合物并促进Ag/TiO2表面质子光还原成氢气。
2.实验步骤
2.1.Ag/TiO2复合光催化剂的制备。采用典型的光沉积的方法使纳米银(NPs)负载到TiO2(P25)表面将0.5 g/L的TiO2水溶液与1 mol/L的甲醇(给电子体)、0.14 mmol/L的AgNO3溶液搅拌超声30分钟。接着用200 W的汞灯照射30分钟,过滤,用去离子水洗涤,在80 ℃的烘箱里干燥。用同样的方法制备Pt/TiO2和Au/TiO2,分别以H2PtCl6和HAuCl4为金属前驱体。利用电感耦合等离子体原子发射光谱(ICP-AES)测量出Ag/TiO2、Pt/TiO2、Au/TiO2光沉积后未使用的前驱体浓度大约为3 %。
将硫氰酸根离子复合Ag/TiO2样品进行高分辨透射电子显微镜(HR-TEM)、拉曼光谱(Raman)、紫外可见吸收光谱(DRS)和X射线光电子能谱(XPS)分析。此外,为分析AgSCN/TiO2的特性,在Ag/TiO2水溶液中加入计算量的硫氰酸钾(KSCN),搅拌3 h,将制得AgSCN/TiO2样品过滤,80 °C烘箱中烘干,并将无硫氰酸根离子的Ag/TiO2以同样的方式制备作为对照样品。
2.2.光催化制氢性能测试。将制备好的Ag/TiO2在耐热玻璃反应器中加入甲醇(作为给电子体)和硫氰酸钾水溶液。接着将悬浮液用氩气净化,超声分散。采用300 W氙光灯作为光源,通过10 cm红外滤光器和紫外滤光 (lambda;gt;320 nm)。在照射过程中,对反应器的顶空气体(大约35 mL)进行了间歇采样,并利用装有热导率检测器和5 Aring;分子筛柱的安捷伦6890A气相色谱仪对氢气进行了分析。在同一个反应器中重复光催化制氢,并在每个光照射循环结束(3 h)和开始下一次循环之前,用氩气净化反应器。
2.3.光催化剂的表征。采用带有图像校正器的型号为JEO JEM2200FS (200 keV,0.1 nm)的扫描透射电子显微镜(STEM)和大角度环形暗场(HHADF)对Ag纳米粒子在TiO2颗粒上的分布进行了表征,并用能量色散X射线能谱(EDS)对其元素分布进行了分析。用带有球面附着体的岛津紫外型号为2401PC分光光度计记录了样品的紫外可见吸收光谱。;硫氰酸根离子吸附Ag/TiO2的表面原子组成的X射线光电子能谱分析光谱(XPS)的数据是以BaSO4为参比,以Mg Kalpha;线(1253.6 eV)为激发源,由Kratos公司的XSAM800pci系统测定的。采用拉曼光谱仪(Horiba Jobin Yvon/Labram ARAMS) 使用514nm激光线(Ar-离子激光器)作为激发源分析了吸附在Ag/TiO2上的SCN-的拉伸振动。用配备有Dionex IonPac AS 16(4 mmtimes;250 mm)的色谱柱和电导检测器的离子色谱(IC,DIONEX DX-120)监测硫氰酸根离子的吸附和降解。
2.4.光电化学的测量。光电化学(PEC)测量是采用与传统的三电极PEC反应器连接的、带有石英窗口的Pyrex电池的恒电位器(Gamry,Reference 600)进行的。负载钛箔的光催化剂、盘绕的铂丝和Ag/AgCl电极分别作为工作电极、对照电极和参比电极。光催化剂电极采用电泳法制备,用厚度为0.127 mm,纯度为99.7%的Aldrich钛箔作为电泳沉积光催化剂的基底。在电泳沉积过程中,用绝缘带覆盖钛箔作为阴极,留下1 cm2的面积的裸钛箔作为阴极,将两种钛箔电极浸入P25或M/TiO2 (M=Pt、Au、Ag)(10g/L)的纯甲醇溶液中,然后在钛箔电极上通25 s的25.0 V的电流进行电沉积。将除去悬浮液的阳极钛箔,在450°C和氩气通入的条件下煅烧30 min。尽管对M/TiO2电极进行处理的温度比M/TiO2粉末态的高(450°C对80°C),但XPS和X射线衍射分析表明,金属的表面氧化状态和TiO2的晶型没有变化。在三电极PEC反应器加入pH为11.0 的NaClO4(0.2M)和甲醇(10 vol%)组成的电解质水溶液,并用氩气连续净化。分别在minus;2.0~1.5 V和minus;1.0 V(相对于Ag/AgCl)的外加偏压下,测量了线性扫描伏安图(LSV)和电化学阻抗谱(EIS)。在pH11.0的NaClO4(0.2M)电解液中测量了开路电位(OCP)。在黑暗(E0)和紫外光照射(Eph)下测量了1000 s后的平衡开路静态电位。为了保证电极行为的重现性,使用了相同的电极和在光催化实验中使用的300W的氙光灯。
3.表征与结果
采用经典的光沉积方法将贵金属(Ag、Pt、Au)负载在TiO2的表面,负载浓度大约为3%。根据图1a所示,以甲醇为给电子体的添加了硫氰酸根离子的Ag/TiO2的制氢量相比于Ag/TiO2提升了四倍左右。对于产氢来说牺牲剂甲醇的存在是十分重要的,当没有甲醇溶液时硫氰酸根离子没有诱导作用,这说明硫氰酸根离子不作为给电子体或电子空穴。另一方面,硫氰酸根离子对于Pt/TiO2和Au/TiO2没有类似的积极影响(图1b和图S1),加入硫氰酸根离子的Pt/TiO2制氢性能略有下降,而Au/TiO2没有明显变化。而在乙醇、乙二胺四乙酸(EDTA)等电子供体的存在下,硫氰酸根离子对H2的生成也有正面的影响(见图2a)。通过改变KSCN含量和银在TiO2的负载量,检测硫氰酸根离子最优含量,结果表明,当KSCN大于0.1 mmol/L,银的负载量大于3.0%时为最优含量(图2b,c)。因此,本实验中大多是在Ag(3%)/TiO2和0.1 mmol/L KSCN的条件下进行的,值得注意的是硫氰酸根离子对于产氢的影响在0.1 mmol/L KSCN的条件下到达饱和刚好与硫氰酸根离子在Ag/TiO2的饱和吸附量一致(图2b)。相反,Pt/TiO2、Au/TiO2和纯的TiO2对硫氰酸根离子几乎没有吸附,这一点证明了硫氰酸根离子在纳米银的吸附和硫氰酸根离子与Ag/TiO2的表面复合是制氢性能提升的原因。由图2d可知在光照过程中硫氰酸根离子的浓度没有完全降低,这表明在过量空穴助剂(MeOH)的存在下,空穴和羟基自由基的反应抑制了硫氰酸根离子的光催化降解。
为了进一步证明硫氰酸根离子的效果,我们还进行了一些控制试验,结果如图3a所示。虽然阳离子的类型不同,但测试的硫氰酸盐试剂(即GSCN(硫氰酸胍)、NaSCN和KSCN)均表现出相同的正效应,从而排除阳离子起作用的可能。与不含硫原子的氰化物(CN-)和氰酸盐(OCN-)结构相似的阴离子只能在很小的程度上改善Ag/TiO2的H2生成活性。这说明硫氰酸根离子的增强效应应该归因于Ag/TiO2与硫氰酸根离子之间的独特的相互作用。同时我们也应该注意到,硫氰酸根离子在Ag/TiO2上增强H2的生成量主要通过重复的光催化循环来维持生成活性,并且很少显示出失活迹象(图3b)。虽然沉积在TiO2上的银可以通过在光照下与空穴反应而发生氧化溶解,但过量的MeOH作为还原剂的存在应该抑制这种溶解反应。
STEM图像(图4)表明,Ag纳米粒子(STEM暗场中的光球)很好地沉积在TiO2颗粒上,Ag 纳米颗粒的平均尺寸约为4纳米(大小范围1~20纳米)。Pt和Au 纳米粒也很好地沉积在TiO2颗粒上(见图S2),但与Ag纳米粒子的尺寸有所不同。Pt纳米粒比Ag纳米粒小(1~3 nm),而Au纳米粒比Ag纳米粒大(3~28 nm)。虽然贵金属纳米颗粒尺寸不同对光催化活性有一定的影响,但本文主要关注硫氰酸根离子在浮在金属TiO2中的相对作用,不应受到由于金属纳米颗粒不同尺寸带来的影响。为了证实SCN-在Ag/TiO2上的吸附,采用点分布EDS(能量色散X射线光谱学)方法对Ag/TiO2和硫氰酸根离子吸附的Ag/TiO2的分析结果如图4e所示(参见图S3的EDS谱图)。点分布EDS谱图证实白色亮球为Ag纳米颗粒,较大不规则形状的颗粒为TiO2。硫氰酸根离子吸附Ag/TiO2的硫元素主要分布在Ag 纳米粒的
全文共7960字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[10552],资料为PDF文档或Word文档,PDF文档可免费转换为Word
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。
您可能感兴趣的文章
- 通过对奥美拉唑合成反应的监测和定量反应的在线拉曼光谱和表征组件外文翻译资料
- 无金属碳基催化剂的研究进展外文翻译资料
- 钼酸钙/碳三维复合材料可控设计合成的研究外文翻译资料
- 生物催化选择性合成功能化喹唑啉酮衍生物外文翻译资料
- 三元V Zr Al ON氧氮化物-3-甲基吡啶氨氧化的高效催化剂外文翻译资料
- 综述纳米零价铁(nZVI)的合成,特性和在环境修复中的应用外文翻译资料
- 自消毒PVC表面使用点击化学设计外文翻译资料
- 微波辅助直接合成4H-1,2,4-苯并噻二嗪1,1-二氧化物衍生品外文翻译资料
- 微波辅助下直接合成1,1-二氧代-4H-1,2,4-苯并噻二嗪类衍生物外文翻译资料
- 压力选择在变压精馏中的重要性外文翻译资料


