
英语原文共 3 页,剩余内容已隐藏,支付完成后下载完整资料
水热合成法制备具有增强的光催化性能的TiO2/Ti3C2纳米复合材料
Yupeng Gao,Libo Wang n,Aiguo Zhou,Zhengyang Li,Jingkuo Chen,Hari Bala,Qianku Hu,Xinxin Cao
摘要:通过水热合成法成功制备了具有高光催化活性的TiO2/Ti3C2纳米复合材料。这种复合材料的微观结构和物相组成由场发射扫描电子显微镜(FESEM)和X射线衍射仪(XRD)来表征。在紫外线照射下,通过分别测试纯相TiO2和TiO2/Ti3C2纳米复合材料对甲基橙(MO)的降解速率来评价其光催化性能。光降解测试结果显示TiO2/Ti3C2复合材料比纯TiO2纳米材料具有更好的光催化活性。实验表明,在紫外光照射下,TiO2/Ti3C2复合材料比纯TiO2或Ti3C2表现出更高效的电子-空穴分离速率。
- 介绍
在过去的几十年里,随着经济的发展,纺织和染料工业的污染物对水生生物和人类是非常危险的[1,2]。近年来,实验发现了金属氧化物半导体具有良好的光催化活性,在光照下可以将有毒的有机物降解为低毒性小分子[3-5]。二氧化钛(TiO2)是一种受到了广泛研究的光催化材料,主要归功于它具有良好的光催化性能,低成本,无毒和简便实用的特点[6-8]。TiO2主要有三种不同的晶型:锐钛矿,金红石和板钛矿,它们拥有不同的能带间隙和化学活性。一般来说,锐钛矿具有比金红石更好的光催化活性,这主要归功于两点,一点是锐钛矿比金红石有更宽的禁带宽度,另一点是锐钛矿的表面能够吸附更多的氧分子,因此它可以有效地抑制电子空穴的结合[9]。然而,TiO2是一种直接能带间隙半导体,它产生的光生电子-空穴对能快速重组,从而降低了它的光催化效率[6,10]。因此,阻止电子-空穴对的复合,提高TiO2的光催化活性是一项巨大的挑战。如今,已可以采用多种方法合成TiO2基纳米复合材料,相比于纯相TiO2,其可以有效地抑制电子-空穴复合或者扩展太阳光的吸收范围,例如使用贵金属基底[11],离子掺杂[12],以及采用半导体[4],金属氧化物[13]或碳材料[14]等复合。特别是,人们越来越关注碳基和二氧化钛的复合材料,主要因为它们具有协同组合效应从而增强了其光催化性能[15]。据报道,分层有序的大介孔TiO2-石墨烯复合物薄膜具有快速吸附和光降解甲基蓝的能力,其表观催化速率几乎是纯介孔二氧化钛薄膜的17倍,这主要是由于石墨烯有效抑制了薄膜中的电荷重组[16]。此外,Ma等人,合成的TiO2/碳纳米纤维复合材料具有良好的光催化性能[17]。
最近,被称为MXenes(一般通式为Mn 1Xn,其中n取1,2或3,M代表过渡金属元素,X代表C或N)的一类新型二维(2D)过渡金属碳化物和碳氮化物被发现了,研究员已经开始合成并研究其独特的性质[18-21]。至今,MXene系列包括:Ti3C2,Ti2C,V2C,Nb2C,(Ti0.5,Nb0.5)2C,Ti3CN,(V0.5,Cr0.5)3C2和Ta4C3[20],其中Ti3C2受到了广泛研究。最近,Michael Naguib等人,在空气中加热二维Ti3C2,得到了嵌入进薄片状无序石墨碳结构中的TiO2纳米晶粒[22]。据我们所知,目前还没有关于TiO2/Ti3C2复合材料合成的报道。
在此,课题组已经成功地采用水热合成法制备了TiO2/Ti3C2纳米复合材料。2D Ti3C2的表面采用锐钛矿TiO2纳米晶粒修饰。由此产生的异质结构在紫外光照射下表现出良好的光催化性能,能高效光降解甲基橙(MO)。
- 实验部分
TiO2/Ti3C2纳米复合材料的制备:首先,在70mL去离子水中溶解特定量的硫酸钛(TiSO4),然后在上述溶液中加入500mg的Ti3C2,溶解。随后,快速搅拌混合物溶液1小时,使前驱物均匀混合,然后转移到100毫升聚四氟乙烯高压釜中。再将反应釜密封,转移放入烘箱,设置温度180℃,保温18小时。待反应釜冷却至室温后,采用离心法分离产物,用去离子水和乙醇洗涤除去可能吸收的离子和剩余的原料,然后在80℃真空中干燥10小时。此后,可以获得并收集TiO2/Ti3C2纳米复合材料,用于测试。
为了方便比较,通过相同的方法制备不含Ti3C2的纯相TiO2。将Ti3AlC2在60℃下、49%HF(阿拉丁试剂,中国)中静置24小时,通过浸渍刻蚀的方法制备纯2D Ti3C2。然后将样品离心分离,用去离子水反复洗涤并在80℃真空下干燥[23]。
光催化试验:在紫外线照射下,通过测试不同样品对甲基橙(20mg/L)的光降解速率来评估光催化能力。对于光催化测量,将100毫克光催化剂样品溶解于100mL甲基橙染料溶液中,并在黑暗中用磁力搅拌器搅拌30分钟,以建立光催化剂与甲基橙MO之间的吸附平衡。整个光催化反应在10℃下发生,此后采用175瓦汞灯产生的光进行辐射照明(GGZ175,中国上海吉光特种照明电器厂),每10分钟取出5毫升溶液,离心除去催化剂,再采用紫外分光光度计进行测试分析(TU-1900,北京普鲁金杰通用仪器公司,中国有限公司)。
表征:采用粉末衍射仪(Bruker AXS公司,德国)获得X射线衍射图案,技术指标:使用Cu的Kalpha;线辐射源,扫描步进设置为每3秒一步,每步0.02°。通过场发射扫描电子显微镜测试样品的形态和微结构(FESEM,Hitachi-S4800,日本)。
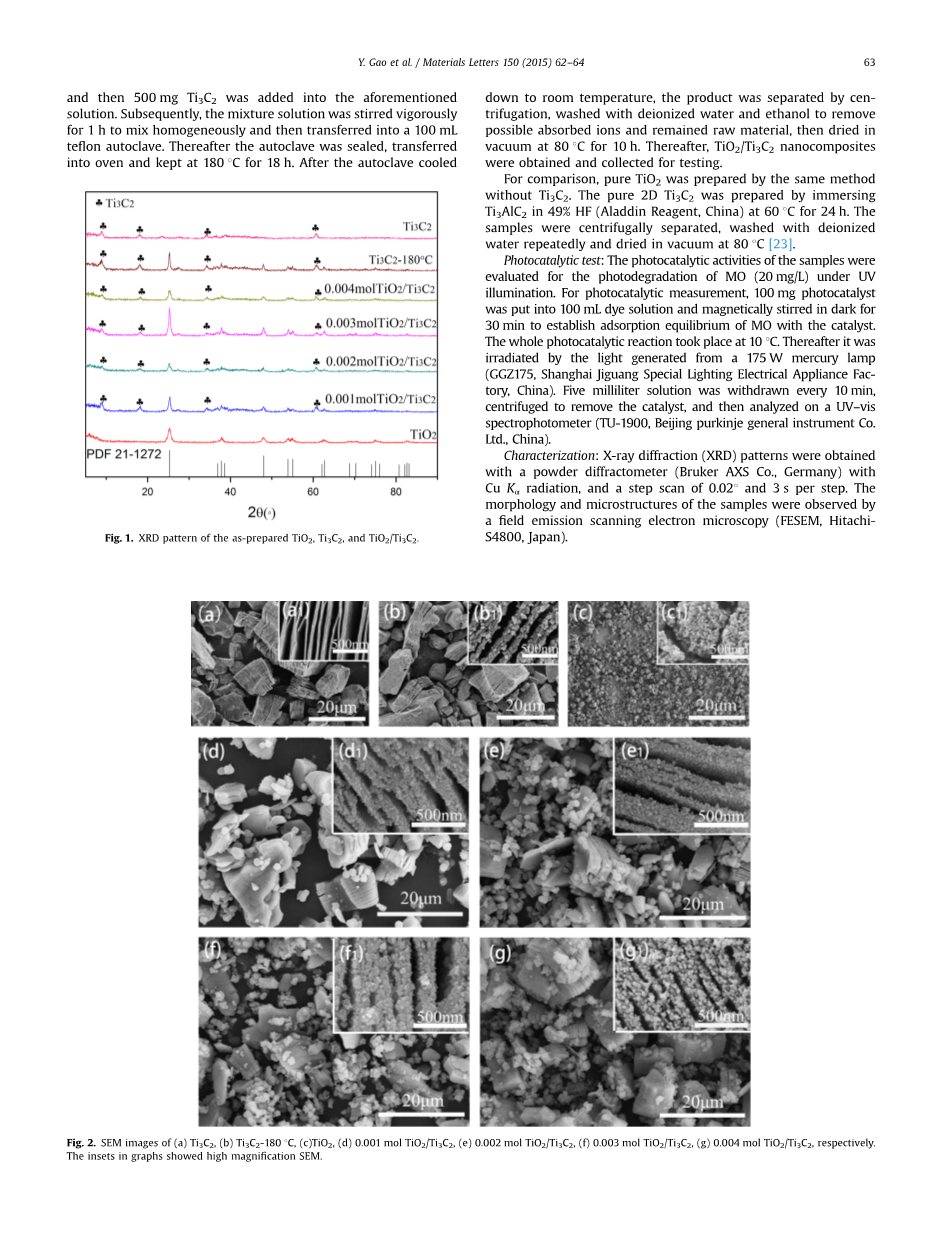
图一:已经制备的TiO2,Ti3C2,和TiO2/Ti3C2的XRD图谱
图二:各种物质的SEM图(a)Ti3C2,(b)Ti3C2-180℃,(c)TiO2,(d)0.001mol TiO2/Ti3C2,(e)0.002mol TiO2/Ti3C2,(f)0.003mol TiO2/Ti3C2,(g)0.004mol TiO2/Ti3C2。右上脚的插图有更高的放大倍数。
图三:各种光催化剂的光催化降解速率(C0/C-t)曲线
- 结果和讨论
图一记录了原始样品Ti3C2,TiO2和TiO2/Ti3C2的X射线衍射图谱,其中衍射角2theta;的范围为5-90°。如图一所示,所有被指标化的衍射峰(底部图案)来源于没有晶相杂志的纯相锐钛矿TiO2(JCPDS 21-1272)。顶部图案来源于纯相Ti3C2,其所有的强衍射峰分布在2theta;=9.0°,18.2°和27.5°,中部图案来源于TiO2/Ti3C2复合材料,兼有锐钛矿和Ti3C2的衍射峰。
图二显示了Ti3C2,TiO2和TiO2/Ti3C2纳米复合材料的SEM图像。图二(a)显示了纯相Ti3C2的SEM图像,Ti3C2显示为层状形态,每层大约40nm厚度。图二(b)中显示了在180℃下制备的Ti3C2样品的SEM图像,Ti3C2纳米片密集排列且其表面不规则地覆盖有成型的纳米颗粒,基于XRD结果(图1),纳米颗粒应该是二氧化钛,这是在180℃下Ti3C2部分氧化形成的。图2(c)显示的为TiO2样品,纯相TiO2产品含有平均尺寸为1-4um的不规则颗粒,它们由许多尺寸大约为30nm的纳米颗粒组成。图2(d-g)显示了TiO2/Ti3C2纳米复合材料的SEM图像。从图像中,可以看到一些球形颗粒,以及在Ti3C2层的边缘存在一些纳米颗粒,这些颗粒与在Ti3C2-180°图像中观察的纳米颗粒不同。与180℃下获得的Ti3C2样品相比,纳米复合材料中的TiO2纳米颗粒更规则,呈球形。同时纯相TiO2样品(图2c)存在明显的团聚现象。这种团聚主要是由于高表面纳米粒子之间的相互作用,这些粒子具有大的比表面积和高表面能。团聚可能发生在干燥过程中。
将光催化降解甲基橙MO作为反应模型,分别测试TiO2,Ti3C2,TiO2/Ti3C2纳米复合材料的光催化活性。图三显示了测试结果,与TiO2和Ti3C2相比,0.001mol,0.002mol和0.003mol TiO2/Ti3C2纳米复合材料具有较高的光催化活性,甲基橙MO在30分钟内迅速降解约98%。0.004mol TiO2/Ti3C2纳米复合材料的光催化效率相对较差。与此同时,尽管具有相同的催化时间,但以纯相TiO2纳米粒子为催化剂的降解率只有77%,纯Ti3C2催化剂的降解率仅42%,在180℃下发生反应的Ti3C2样品的光催化效率是最糟糕的。此外,实验发现纯Ti3C2也有某些光催化性能。这些实验现象表明,在紫外光照射下TiO2/Ti3C2纳米复合材料比纯TiO2和Ti3C2表现出更高的电子-空穴分离效率,这可能是因为TiO2和Ti3C2之间形成了异质结。
- 结论
本文展示了一种制备TiO2/Ti3C2纳米复合材料的全新方法。测试显示T
全文共5618字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[1390]
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。
您可能感兴趣的文章
- 基于电纺Ti02纳米纤维的超灵敏化学电阻器外文翻译资料
- Cu/还原氧化石墨烯复合材料的合成、表征及摩擦学性能外文翻译资料
- 显著地阻碍无电镀的Ni-W-P金属喷镀和无铅Sn-3.5Ag焊接之间的界面反应外文翻译资料
- 纳米稀土氧化物改性复合聚合物电解质的制备及性能研究外文翻译资料
- 高速大气等离子喷涂在铜表面沉积钨涂层的性能研究外文翻译资料
- 制备条件对纳米多孔铜形态和热稳定性的影响外文翻译资料
- Fe-Cr-Mo三元合金相分离的计算机模拟外文翻译资料
- 通过不同的纳米尺寸Y TZP形成悬浮液的流变性的研究外文翻译资料
- 碳钢制备及溶胶-凝胶法Al2O3/Ni-P的表面复合镀层外文翻译资料
- 基于掺杂纳米铜粒子硅基溶胶的超疏水抗菌棉织物表面的制备外文翻译资料


