
英语原文共 6 页,剩余内容已隐藏,支付完成后下载完整资料
纳米BaCO3和TiO2固相合成超细BaTiO3粉体
通过纳米TiO2(70nm)与不同粒径(650、140和50nm)BaCO3的固相反应制备了钛酸钡。结果表明,BaCO3的粒径对钛酸钡的固相合成有很大的影响。使用纳米晶BaCO3已经导致在800C下焙烧8小时后形成单相BaTiO3。最终粉体由100nm初生粒子组成,粒径分布窄,d50=270nm,团聚体不大于800nm。对于较粗的碳酸氢盐,需要在1000℃煅烧4h,而最终粉末则要粗得多。纳米晶BaCO3和TiO2的固相反应是制备BaTiO3超细粉末的化学预处理途径的一个替代方案。
- 简介
本文介绍了铁电材料、多晶钛酸钡(BaTiO3)由于其相对介电常数(Er)较高,损耗较低,在电子工业中应用广泛(年产量:11000吨),尤其是在多层陶瓷钙离子电池(MLCC)中,作为电介质在陶瓷电容器中广泛应用。BaTiO3基材料的其他应用包括压电器件、电致发光板、热电元件、用于印刷电路内嵌钙的聚合物基复合材料电路板,带正温度系数电阻率(PTCR)的加热器和传感器等。最近,在单晶BaTiO3中实现大的电应变效应的可能性已经显现出来,这可能会产生新一代的致动器。
随着微电子技术和电子通讯技术的不断进步,铁电体元件和多层电池正逐步向小型化发展。陶瓷电容器在两个方向上继续发展:体积较小的组件和更大的电容值。为了在小体积内获得高电容,必须在增加总层数的同时减小介电层厚度。在不久的将来,介电层厚度将le;1mu;m,层数可能超过1000层。因此,人们对粒径小(100~300nm)、粒度分布窄的高质量BaTiO3粉体的关注不断增加。传统的BaTiO3基材料是由BaCO3与TiO2之间的高温固相反应制备的。这种方法通常产生相对粗糙和团聚的颗粒,不适合处理薄介电层的MLCC。在水中强化研磨BaTiO3,减小粒径,使Ba2 浸出,pH值升高,不利于进一步加工。已有数种制备精细和弱团聚粉体的化学路线。然而,这些方法大多比固态反应昂贵,有些方法有明显的缺点。特别是,水热法或溶液沉淀法制备的粉末通常含有晶格羟基,导致烧结MLCC过程中产生不理想的孔隙。因此,通过固态反应,研究具有窄尺寸分布的BaTiO3粉体的可能性,是一项非常科学和实用的研究。固相BaTiO3的制备基于以下反应
(1)
从通过热重分析(TGA)收集的重量损失数据或通过X射线衍射作为时间和温度的函数研究该过程的动力学,并且建议固态扩散作为控制反应速率的最可能机制。反应过程与TiO2的性质(即金红石或锐钛矿)无关。在扩散偶合实验的基础上,Beauger等人提出BaTiO3的生长受钡离子通过钙钛矿层的扩散控制。结果,BaTiO3层在TiO2的表面上发展并且通过母体颗粒的逐渐消耗而向内生长。最近已经通过拉曼光谱成像证实了这种机制,其是在较大TiO2颗粒表面涂覆有BaCO3壳的情况下作为温度的函数。因此,预期最终BaTiO3颗粒的尺寸和形状主要由起始TiO2的形态决定。我们使用不同尺寸的TiO2颗粒有效地观察到了这种相关性。因此,原则上可以使用合适的纳米晶体TiO2原料制备非常细的BaTiO3颗粒。最近研究已经表明,利用目前市场上大量且价格相对较低的高质量纳米晶锐钛矿和金红石粉末,使用减少核心固态反应的概念,可以由相对粗的BaCO3和纳米晶ZrO2制备非常细的BaZrO3粉末。然而,当以粗碳酸盐为原料时,反应(1)通常需要1000℃-1100℃的温度才能得到单相产物。在此条件下,TiO2和BaTiO3纳米晶粒子会发生快速粗化和聚集,使用一种非常细的TiO2前驱体具有潜在的优势。
关于BaCO3粒径对BaTiO3的固态形成的影响知之甚少。如果反应动力学是由固态扩散唯一确定的,那么预计只会产生较小的影响。相反,Hennings等人报告,亚微米BaTiO3前体的使用会使得具有单相钙钛矿所需的反应温度降低。因此,必须重新考虑BaCO3在溶胶态合成BaTiO3中的作用。本研究的目的是研究用纳米晶原料进行固态反应的具有窄PSD的超细(100nm)BaTiO3粒子的合成。特别注意了BaCO3颗粒大小对反应动力学的影响。
- 实验
化学计量数量的纳米晶体TiO2(Toho Titanium, Chigasaki, Japan, HT2301, SBET =22.5 m2/g, dBET =67nm, d50 =170nm)标准BaCO3(Solvay Bario e Derivati, Massa, Italy, VL700S, SBET =2.1 m2/g, dBET =655nm, d50 =1290nm)亚微米BaCO3(Solvay Bario e Derivati, BM040, SBET =10.4 m2/g, dBET =136nm, d50 =170nm),和纳米 BaCO3(Solvay Bario e Derivati, BM020, SBET =31.2 m2/g, dBET =48nm, d50 =11 nm)使用ZrO2介质,将BaCO3在聚乙烯罐中的水中充分混合。加入聚丙烯酸铵盐溶液(Acros Chimica, Milan, Italy, MW 2000)作为分散剂。聚合物的浓度要求在颗粒表面形成单层。制备了三份不同的混合物,分别为纳米晶BaCO3(BT1)、亚微米BaCO3(BT2)和标准BaCO3(BT3)。所有原材料均为工业数量的电子级产品。TiO2粉体由62%金红石和38%锐钛矿组成的70nm聚集球形颗粒组成。碳酸钡粉体由针状晶体组成,其纵横比随比表面积的增加而增大,从2增加到10。混合后,在110℃的烘箱中干燥,最后过筛(80目)。BaCO3和TiO2在背散射(BS)电子模式下有着截然不同的灰度对比度,易于分辨。所有混合物的混合的水平相当好。对于BT1,在200 mm x 200 mm的区域内只观察到少量的小团聚体,这些团聚体的尺寸lt;1mu;m。这些残留附聚物对固态反应的影响可以认为是微不足道的。
采用热重法和差热分析法研究了TiO2与BaCO3的反应动力学(TG/DTA, Setaram LabSys, Caluire, France)。在100kPa(1atm)的压力下,在0.1L/min的干燥空气下,以5℃/min加热混合物至1300℃。第二种类型的TG/DTA实验通过快速加热混合物进行(20℃/min)并在预设温度下进行保温。分别在700℃、800℃和900℃条件下进行等温运行。有机分散剂的完全燃尽是在400℃等温保温2h完成的。在加热速率为5℃/min,保温时间不同的条件下,研究了箱式炉中BaTiO3的形成过程。上述部分实验在4kPa(0.04atm)的压力下重复。用X射线衍射法(XRD, CoKa radiation, Philips PW1710, Philips, Eindhoven, The Netherlands)对煅烧粉体进行了相组成和衍射分析。用扫描电镜(SEM, LEO 1450VP, LEO Electron Microscopy Ltd., Cambridge, UK)对原料和最终煅烧粉体的形貌进行了表征。根据BET法,通过氮气吸附测量比表面积(SBET)。(Micromeritics ASAP 2010, Micromeritics, Norcross, GA)用氦显象限法(Micromeritics Accupyc 1330)测定了粉末的密度rho;。计算出等效化BET直径dBET = 6/rho;SBET。用X射线圆盘光离心机测量了颗粒的粒度分布。(BI-XDC, Brookhaven Instruments Corp, Holtsville, NY)。以5℃/min的升温速率在空气中以1145℃、1200℃、1225℃、1250℃和1300℃在空气中烧结最终单相BT1粉末。用100MPa的冷等静压法制备生坯。未添加粘合剂或烧结助剂。得到的陶瓷的密度是通过阿基米德的方法获得的,以化学刻蚀后抛光表面的平均截距长度来确定晶粒尺寸。
- 结果
(1)TG/DTA
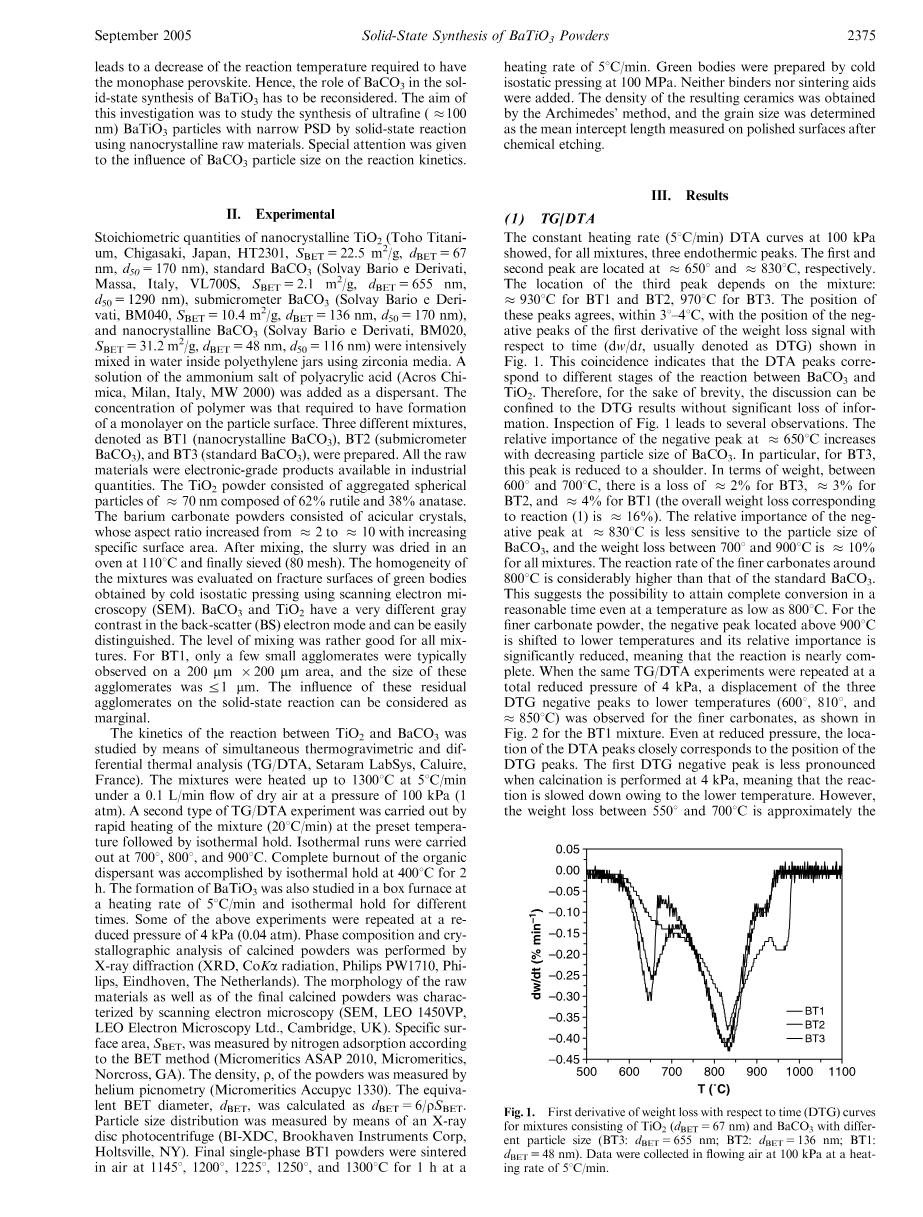
在100kPa下,恒定升温速率(5℃/min)DTA曲线显示出三个吸热峰。第一和第二峰分别位于650℃和830℃。第三个峰的位置取决于混合物:930℃的BT1和BT2,970℃的BT3。这些峰的位置在3℃-4℃范围内与相对于时间(dw/dt,通常表示为DTG)的重量损失的导数的第一个负峰的位置一致。如图1所示。这表明DTA峰对应于BaCO3和TiO2反应的不同阶段。
因此,为了简洁起见,本文的讨论可以在不引起重大信息损失的情况下对最终的结果进行讨论。对图1的观察显示:在650℃下,负峰值的相对重要性随着BaCO3的粒径的减小而增加。特别地,对于BT3,该峰值被减小到肩部。就重量而言,在600℃至700℃之间,BT3损失2%,BT2损失3%,BT1损失4%(反应(1)的总失重率为16%)。830℃负峰的相对重要性对BaCO3的粒径不太敏感,700℃~900℃之间的失重率为10%。在800℃附近,较细碳酸盐的反应速率明显高于标准BaCO3。这意味着有可能在合理的时间内实现完全转换,即使是在温度低到800℃的条件下。对于较细的碳酸盐粉末,位于900℃以上的负峰移到较低的温度,其相对重要性显著降低,这意味着反应几乎完全。当相同的TG/DTA实验在总压为4kPa时,观察到更细的纳碳酸盐三个DTG负峰向低温(600℃、810℃和850℃)的位移。如图2所示的BT1混合物。即使在减压下,DTA峰的位置也与DTG峰的位置密切对应。当在4kPa进行煅烧时,第一个DTG负峰不明显。由于温度较低,反应速度减慢。然而,在这两种压力下,550℃到700℃之间的失重量大致相同。第二个负峰的深度表明,在压力降低时,在800℃附近反应更快。在4kPa,时负峰在较高温度下几乎消失。
图1 不同粒径的TiO2(dBET =67nm)和BaCO3混合物(BT3: dBET=655nm; BT2: dBET=136nm; BT1: dBET=48nm)的失重时间(DTG)曲线的一阶导数。数据在100kPa流动空气和5℃/min的加热速率下获得。
图2 在100kPa和4kPa空气中TiO2(dBET=67nm)与BaCO3(dBET=48nm)反应的失重曲线的一阶导数(DTG)曲线。
(2)等温反应动力学
反应物比例可以由下式计算
其中w0为初始重量,wt为时间t的重量,winfin;是反应(1)完成时的理论重量。在不同温度下,混合物BT1和BT3的反应动力学如图3。BaCO3粒度的影响很明显:从纳米晶获得的混合物BaCO3的活性明显高于粗碳酸盐的混合物,在800℃下反应8h后反应分数达到100%。随着温度的升高和反应时间的增加,差异逐渐减小。因此,在900℃时,所有混合物在8h后都发生完全转变,值得注意的是从减重测量中获得的反应动力学数据描述了二氧化碳的演变,但总的来说,如果其他三元化合物(如Ba2TiO4)在反应过程中出现的话,则这并不能完全对应
全文共8923字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[1346]
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。
您可能感兴趣的文章
- 复杂热电材料外文翻译资料
- 以自蔓延高温烧结方法制备热电化合物以及燃烧合成的新标准外文翻译资料
- 氮掺杂分级多孔碳作为氧还原反应的高效电化学催化剂的研究外文翻译资料
- 孪晶诱导塑性高嫡合金的设计外文翻译资料
- 含铌先进Fe-Cr-Ni型奥氏体耐热钢富铜相的析出强化在超临界电厂的应用外文翻译资料
- 不同温度下直接能量沉积层状工具钢的弯曲强度外文翻译资料
- BiFeO3的光伏效应外文翻译资料
- 通过氢稳定的MgaPt研究核壳纳米结构Mg@Pt中快速“氢泵”的可视化外文翻译资料
- 一种铱核心环金属有机配体显著地提高了有机太阳能电池 的光伏性能外文翻译资料
- 钠离子电池的高性能阳极材料:三组分共组装法制备层次多孔碳外文翻译资料


