
英语原文共 6 页,剩余内容已隐藏,支付完成后下载完整资料
燃烧合成Nb2O5-Al-Al4C3粉末压坯制备Nb2AlC的研究
摘要
以Nb2O5-Al-Al4C3粉末压块自蔓延高温合成(SHS)为模式,通过燃烧合成法制备了层状三元碳化物Nb2AlC。通过采用两个系列的样品化学计量来研究Al和Al4C3的含量对产物组成和燃烧行为的影响,所述两个系列的样品化学计量比为3:9:1至3:13:1(用于提供额外的Al)和Nb2O5:Al:Al4C3 3:9:1至3:9:1.6(对于额外的Al 4 C 3)。当与Nb2O5:Al:Al4C3 = 3:9:1的粉末压块相比时,Al或Al4C3的增加降低了燃烧温度,从而减缓了燃烧前沿。然而,含有适量的Al或Al4C3的样品有效地改善了Nb2AlC的形成。在本次研究中,从Nb2O5:Al:Al4C3 = 3:11:1和3:9:1.1比例的粉末压坯中获得了Nb2AlC的最佳变化。除Nb2AlC和Al2O3外,二元碳化物NbC始终存在于最终产品中。 Al或Al4C3的进一步增加导致形成Nb4AlC3和NbAl3,并且随着Al4C3的含量过量,NbC的量显着增加。因此,对于Al4C3含量较高的样品,如Nb2O5:Al:Al4C3 = 3:9:1.5和3:9:1.6,NbC被认为是最终产品中唯一的碳化物。如此合成的Nb 2 AlC晶粒典型为板状并且与层压微结构紧密堆叠。
关键词:陶瓷 X射线衍射SEM Nb2AlC 燃烧合成
1.简介
三元化合物Mn 1AXn,其中n = 1,2或3,M是早期过渡金属,A是A族(主要是IIIA和IVA)元素,X是C或N,是一类新的 材料结合了金属和陶瓷的优点[1,2]。 它们相对较软,耐损伤性强,抗热震,导电和导热,弹性刚性好,易于加工[1-10]。 它们也具有高强度,高杨氏模量和相对较低的热膨胀系数[1-10]。 这种独特的性质部分来自于键合的金属性质,部分来自分层结构,部分来自于它们的基面位错在所有温度下都是可移动的[10,11]。
在211个最大化合物(n = 1)中,Ti2AlC是代表性成员,并且已被广泛研究[12-16]。除了Ti2AlC外,211 MAX族中的许多碳化物也引起了越来越多的关注,包括Cr2AlC [17-19],Nb2AlC [20,21],V2AlC [22,23],Ta2AlC [24,25],Ti2GeC [26] ,和Cr2GeC [27]。对于这项工作的特别兴趣是Nb2AlC,它不仅具有良好的机械性能和热性能[9,10,20,21],而且在薄膜形式[28]中也具有400 mK的超导转变[28]。在Nb-Al-C体系中,只有Nb2AlC和Nb4AlC3被确定为MAX相[29,30]。通过使用Nb,石墨和Al4C3粉末,Salama等人[20]通过反应热等静压(HIP)在1600℃和100兆帕8小时制造Nb2AlC。 Zhang等人文献[21]采用原位反应/热压法,在1650℃30 MPa下,从NbC,Nb和Al的粉末混合物中制备Nb2AlC,时间为90 min。在1700℃退火Nb2AlC [29],或在1650℃[30]通过Nb,Al和碳黑粉末的放电等离子烧结来实现Nb4AlC3的生产。
当与反应性HP和HIP方法比较时,自蔓延高温合成(SHS)模式下的燃烧合成利用了高放热反应的自持能力,因此具有低能量需求的潜力,处理时间和设施简单[31,32]。此外,SHS技术已成功应用于制造许多三元碳化物,如Ti3SiC2 [33,34],Ti3AlC2 [35,36],Ti2AlC [16]和Ta2AlC [25]。然而,Nb2AlC尚未通过其组成元素的固态燃烧合成,主要是因为Nb和Al或碳黑之间反应的放热性较弱[37,38]。作为第一次尝试,本研究旨在通过在SHS模式下由Nb2O5,Al和Al4C3的粉末混合物燃烧合成制备Nb2AlC。采用Nb2O5作为铌源的目的有两个:一个是利用Al和Nb2O5之间的铝热反应所产生的大量热量[39,40]。另一种是生成Al2O3作为Nb2AlC的增强体。已经表明,将Al 2 O 3引入MAX碳化物可以改善它们的硬度,韧性和强度[41,42]。特别是,研究了样品化学计量学对Nb2AlC形成的影响,以及反应前沿的燃烧温度和传播速度。在合成产物的相组成的基础上,研究了在Nb2O5-Al-Al4C3体系中固态燃烧形成Nb2AlC的反应机理。
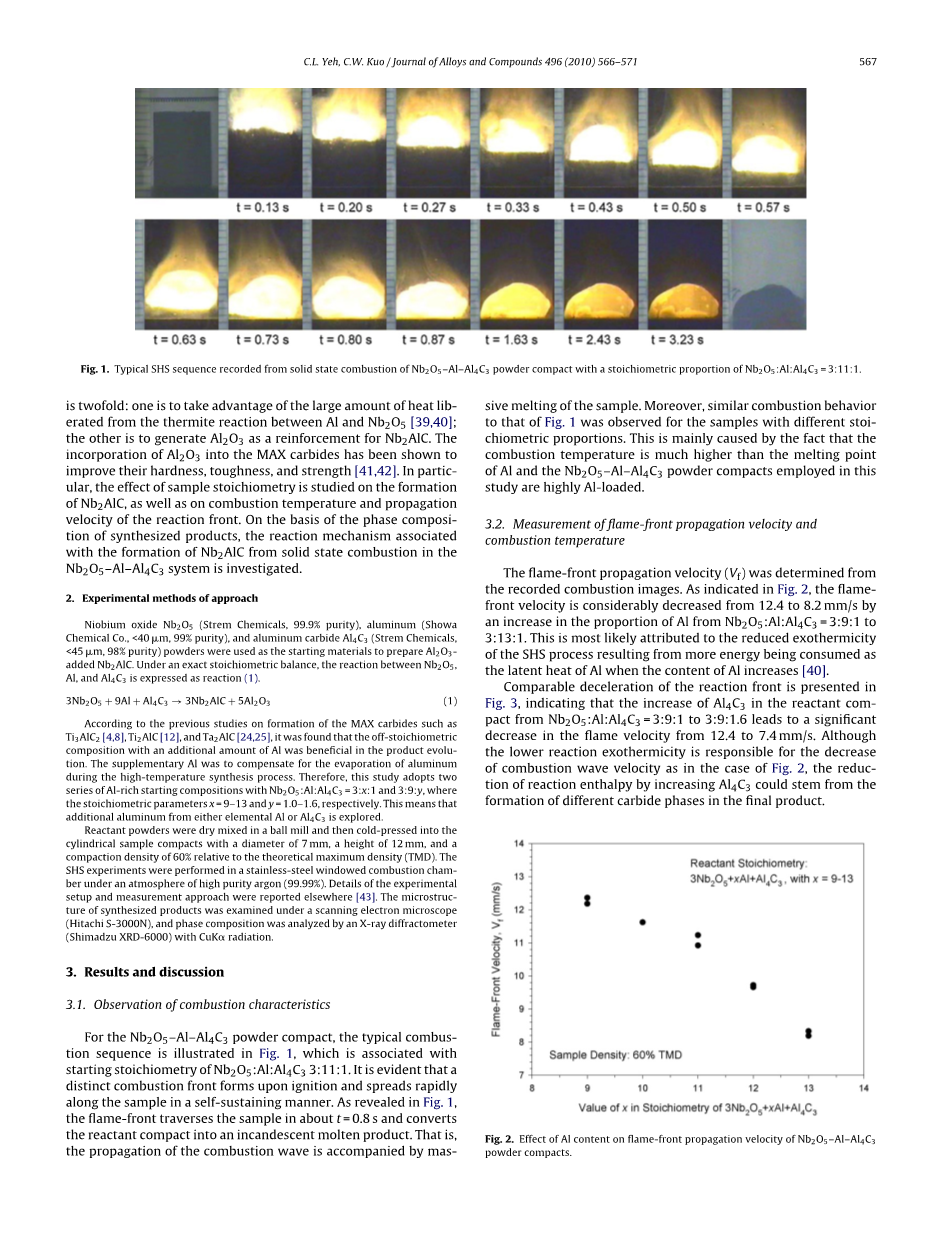
图1.由Nb2O5-Al-Al4C3粉末压坯的固态燃烧记录的典型SHS序列,其化学计量比例为Nb2O5:Al:Al4C3 = 3:11:1。
2.实验方法
氧化铌Nb 2 O 5(Strem Chemicals,纯度99.9%),铝(昭和化学公司,lt;40mu;m,99%纯度)和碳化铝Al 4 C 3(Strem Chemicals,lt;45mu;m,纯度98%)粉末用作起始材料以制备添加Al2O3的Nb 2 AlC。 在精确的化学计量平衡下,Nb2O5,Al和Al4C3之间的反应表示为反应(1)。
3Nb2O5 9Al Al4C3 → 3Nb2AlC 5Al2O3 (1)
根据之前关于形成MAX碳化物如Ti3AlC2 [4,8],Ti2AlC [12]和Ta2AlC [24,25]的研究,发现具有额外量Al的非化学计量组成是有利的 在产品演变中。 补充铝是为了补偿铝的蒸发
在高温合成过程中。 因此,本研究采用了两组富含Al 2 O 3:Al:Al 4 C 3 = 3:x:1和3:9:y的起始组合物,其中化学计量参数分别为x = 9-13和y = 1.0-1.6。 这意味着探索来自元素Al或Al4C3的额外铝。
反应物粉末在球磨机中干混,然后冷压入反应器中相对于理论最大密度(TMD),直径为7mm,高度为12mm,压实密度为60%的圆柱形样品坯块。 SHS实验是在不锈钢窗式燃烧室内,在高纯度氩(99.99%)气氛下进行的。 实验装置和测量方法的细节在别处报道[43]。 在扫描电子显微镜(Hitachi S-3000N)下检查合成产物的微观结构,并通过具有CuKalpha;辐射的X射线衍射仪(Shimadzu XRD-6000)分析相组成。
3.结果与讨论
3.1.燃烧特性的观察
对于Nb2O5-Al-Al4C3粉末压块,典型的燃烧顺序如图1所示,其与Nb2O5:Al:Al4C3 3:11:1的起始化学计量关联。 很明显,点火时形成明显的燃烧前沿,并以自持方式沿样品快速扩散。 如图1所示,火焰前锋在t = 0.8 s左右横穿样品,将反应物压缩物转化为白炽熔融产物。 也就是说,燃烧波的传播伴随着样品的大量熔化。 此外,对于具有不同化学计量比例的样品,观察到与图1类似的燃烧行为。 这主要是由于燃烧温度比Al的熔点高得多以及在本研究中使用的Nb2O5-Al-Al4C3粉末成型体是高Al负载的。
3.2.火焰前缘传播速度和燃烧温度的测量
火焰前沿传播速度(Vf)由记录的燃烧图像确定。 如图2所示,由于Al的比例从Nb2O5:Al:Al4C3 = 3:9:1到3:13:1的比例增加,火焰前缘速度从12.4显着降低到8.2 mm / s。 这很可能是由于当Al含量增加时,由于Al的潜热消耗更多的能量而导致的SHS工艺的放热性降低[40]。
图2 Al含量对Nb2O5-Al-Al4C3粉末压坯火焰前沿传播速度的影响。
图3给出了反应前沿的可比较的减速度,表明反应物中Al4C3的含量从Nb2O5:Al:Al4C3 = 3:9:1增加到3:9:1.6会导致反应物中的Al4C3的显着减少 火焰速度从12.4到7.4毫米/秒。 虽然较低的反应放热率是造成燃烧波速降低的原因,如图2所示,但通过增加Al4C3减少反应焓可能来自最终产品中不同碳化物相的形成。
图3 Al4C3含量对Nb2O5-Al-Al4C3粉末坯块火前传播速度的影响。
在图1和图2中描绘了由不同化学计量的样品记录的燃烧温度曲线。 4和5,分别考虑Al和Al4C3含量的影响。 在温度曲线中观察到的急剧上升意味着迅速燃烧波的到达和峰值对应于火焰前端温度。 如图1和2所示。 如图4和5所示,燃烧温度的组成依赖性与反应前沿速度一致。 当元素Al从Nb2O5:Al:Al4C3 = 3:9:1增加到3:13:1时,燃烧波温度从1774降低到1222◦C可以在图4中看到。同样, 图5显示当样品压块中Al4C3的含量增加时,火焰前端温度显着降低。
图4 Al含量对Nb2O5-Al-Al4C3粉末压坯燃烧温度的影响。
图5. Al4C3含量对Nb2O5-Al-Al4C3粉末压块燃烧温度的影响。
3.3燃烧产物的组成和形态
图6(a) - (c)显示了不同比例的元素铝合成的最终产品的XRD图谱。除了Al2O3与Nb2O5发生铝热反应的副产品外,合成后的产品通常还含有Nb2AlC以及NbC。图6(a)显示了由NbC占主导地位的两种碳化物(Nb2AlC和NbC)以及来自Nb2O5:Al:Al4C3 = 3:9:1样品的一种金属间化合物Nb2Al的形成。二元碳化物NbC和氨化物Nb2Al被认为是Nb2AlC合成中最重要的中间体。根据图6(a),似乎需要更多的Al将NbC转化为Nb2AlC。如图6(b)所示,Nb2O5:Al:Al4C3 = 3:11:1(x = 11)的粉末压块实现了Nb2AlC的演变。此外,图6(b)显示在最终产品中没有检测到金属间化合物。然而,随着Al的进一步增加,图6(c)显示在x = 12时,产品中存在三种碳化物(NbC,Nb2AlC和Nb4AlC3)和一种富Al的铝化物NbAl3。这意味着相转变的恶化,可能是由于反应中过量的Al引起的。如表1所示,从Nb2O5:Al:Al4C3 = 3:11:1样品中获得具有最佳组成的合成产物。 NbC与Nb2AlC的共存主要是由于它们具有特定的取向关系而具有一致的界面结构,正如Lin和他的同事[44-47]对各种三元碳化物和氮化物的显微组织研究所描述的。 NbC和Nb2AlC之间密切的结构关系使NbC在Nb2AlC形成过程中生长。
图6.(a)x = 9,(b)x = 11,(c)x = 13时,由3Nb2O5 xAl Al4C3粉末压块燃烧合成的产物的XRD图谱。
|
Phase composition of SHS products Dominant carbide Secondary carbide(s) |
|
|
NbC |
Nb2AlC |
|
Nb2AlC |
NbC |
|
Nb2AlC |
NbC |
|
Nb2AlC |
Nb4AlC3, NbC |
|
Nb2AlC |
Nb4AlC3, NbC |
表格1 SHS产品相对于Al含量不同的初始化学成分的相组成的总结。
当与Nb2O5:Al:Al4C3 = 3:9:1(y = 1)样品比较时,图7(a)显示Al4C3的轻微增加(y = 1.1)显着提高了Nb2AlC的收率。然而,Nb4AlC3和NbAl3的存在分别在图7(b)和(c)中分别表示Al4C3在y = 1.25和1.3时的初始比例。此外,发现在Nb2O5:Al:Al4C3 = 3:9:1.3的情况下,主要碳化物可能从Nb2AlC转变为Nb4AlC3。如图7(d)所示,Al4C3的进一步增加导致NbC作为最终产品中唯一的碳化物相形成,这对应于Nb2O5:Al:Al4C3 = 3:9:1.5的化学计量比。表2给出的详细总结表明,就Al4C3的含量而言,Nb2O5:Al:Al4C3 = 3:9:1.1和3:9:1.2的粉末压实体更有利于通过固体生产Nb2AlC状态燃烧。根据代表XRD峰的积分强度,表3列出了在最终产物中形成的三种碳化物相(Nb2AlC,Nb4AlC3和NbC)的计算相对含量。如表3所示,在Nb 2 O 5:Al:Al 4 C 3 = 3:9:1的情况下,Nb 2 AlC的相对量(约52%)略大于NbC的相对量(约48%)。通过Nb2O5:Al:Al4C3 = 3:11:1的样品压实实现了Nb2AlC的最高含量达到95%。对于起始比例为Nb2O5:Al:Al4C3 = 3:9:1.3的样品,两种三元碳化物Nb2AlC和Nb4AlC3以相当的量形成,并且它们以NbC为主。最后,NbC是由Nb2O5:Al:Al4C3 = 3:9:1.5反应物压实体产生的唯一碳化物相。
|
Stoichiometry Nb2 全文共8747字,剩余内容已隐藏,支付完成后下载完整资料 资料编号:[9687],资料为PDF文档或Word文档,PDF文档可免费转换为Word |
您可能感兴趣的文章
- 复杂热电材料外文翻译资料
- 以自蔓延高温烧结方法制备热电化合物以及燃烧合成的新标准外文翻译资料
- 氮掺杂分级多孔碳作为氧还原反应的高效电化学催化剂的研究外文翻译资料
- 孪晶诱导塑性高嫡合金的设计外文翻译资料
- 含铌先进Fe-Cr-Ni型奥氏体耐热钢富铜相的析出强化在超临界电厂的应用外文翻译资料
- 不同温度下直接能量沉积层状工具钢的弯曲强度外文翻译资料
- BiFeO3的光伏效应外文翻译资料
- 通过氢稳定的MgaPt研究核壳纳米结构Mg@Pt中快速“氢泵”的可视化外文翻译资料
- 一种铱核心环金属有机配体显著地提高了有机太阳能电池 的光伏性能外文翻译资料
- 钠离子电池的高性能阳极材料:三组分共组装法制备层次多孔碳外文翻译资料


