英语原文共 7 页
SNCR 去除NOx 过程中NH3,NO和O2 在CaO表面吸附和反应的机理研究
施福龙,宋强uArr;,羌瑶
摘要;CaO显著影响SNCR deNOx 过程。研究了NH3 NO O2 体系在CaO表面的吸附和反应机理。结果表明,NH3 吸附在CaO的路易斯酸位点,主要的物种为NH2 和OH。随着温度的升高,NH2 脱氢发生并形成二氮杂,最终解吸为N2O;而OH与H反应形成H2O。O2 加速NH3 转化为NH2 和氧化的二氮化物。CaO表面上没有ad-物种是顺式二聚体亚硝基和单齿硝酸盐。随着温度升高,顺式二聚体亚硝基分解并解析为NO,单齿硝酸盐最终解吸为N2O。O2 对NO ad物种没有影响。当NH3 和NO共存时,它们同时吸附在CaO表面上并通过其单一吸附形成相似的ad-种类。通过NH2将NO还原为N2 ,并且该反应遵循Langmuir-Hinshelwood机制。NH2 与NH3 NO系统中的NO还原同时发生与二氮化物的解离。在NH3 NO O2 系统中,通过O2测定NH3 向NH2 的转化。大部分NH2 被O2氧化,其余部分与NO反应。在O2存在下,NH2 与二氮化物的解离可忽略不计。
1.介绍
氮氧化物(NOx)是重要的空气污染物。水泥窑和循环流化床锅炉(CFBB)排放大量NOx [1,2].考虑到成本和deNOx 效率,选择性非催化还原(SNCR)技术是最适合水泥窑中NOx 控制的技术,也广泛用于CFBB[3,4].已经充分研究了气相SNCR反应的机理。温度,停留时间和混合程度是影响deNOx 效率的因素[5,6].预煅烧炉和旋风分离器是水泥窑和CFBB中SNCR deNOx 工艺的最合适位置。它们为混合和反应提供适当的温度和足够的停留时间。然而,预煅烧炉中Ca基颗粒(主要是CaO和CaCO3)的浓度可以高达出口处1kg / m3 和CaO的比例可为90%[7].含有大量CaO的高浓度循环床材料也存在于旋风分离器中[8].之前的学习[9] 表明CaO催化NH3 氧化并降低SNCR deNOx 过程的效率。因此,当SNCR deNOx 工艺应用于水泥窑和CFBB时,必须考虑CaO的影响。
CaO对NH3 NO O2 体系的影响已经存在研究。人们普遍认为CaO主要催化NH3 氧化,对NH3的NO还原没有影响。因此,CaO降低了SNCR deNOx 过程的deNOx 效率。NH3 转化率和CaO催化的NH3 氧化的NO选择性受温度,NH3和O2 浓度的影响。同时,CaO对NH3 分解具有催化作用,而在不存在O2 时具有NO还原作用[10–12].
然而,NH3 NO O2 体系在CaO表面的吸附和反应机理研究仍然有限,有些结论存在冲突。海赫斯特[13] 使用TGA研究了CaO和NH3 之间的反应,并且基于重量损失数据指出中间产物是Ca3N2 。齐尔马[10] 使用固定床反应器研究了CaO催化的NH3 氧化。推测CaO首先与NH3 反应生成CaN,并且CaN被O2 氧化形成NO。唐[11] 和傅[12] 利用漫反射红外光谱研究了NH3 在CaO表面的吸附
红色傅立叶变换光谱(DRIFTS)。发现NH3 吸附产物为NH2,证明NH3 吸附在CaO表面的路易斯酸位点上。扬子吸附NH3 的DRIFTS研究[14] 还发现轻微的NH 产生,
这表明在CaO表面上存在布朗斯台德酸位点。清水[15] 研究了在CO2 存在下CaO和NH3 之间的反应,并在产物中发现了尿素。因此,NH2 被认为是CaO表面上NH3 转化的重要中间产物。NO吸附和在CaO表面上的反应的研究很少。唐氏对NO吸附的DRIFTS研究[11] 发现顺式二聚体亚硝基是主要的物种。到目前为止,NH3 和NO在CaO表面在不同温度下的吸附和转化仍不清楚。NH3 和NO的共吸附,O2的影响,NH3 NO O2 体系对CaO表面的反应机理尚未见报道。
CaO具有催化活性,在旋风分离器和预煅烧炉中浓度较高,因此,CaO对SNCR deNOx 过程的影响不容忽视。吸附和反应机理对于研究CaO参与的SNCR deNOx 过程非常重要。本研究采用DRIFTS和TPD研究了NH3 NO O2 体系在CaO表面的吸附和反应机理。该结果有助于SNCR技术在水泥窑和CFBB中的应用。
2.试验
在水泥窑和CFBB中,石灰石被注入炉中并在高温下分解成CaO。因此,分析 -
将纯CaCO3 在900℃下煅烧2小时,得到CaO样品,其类似于实际过程中的样品。
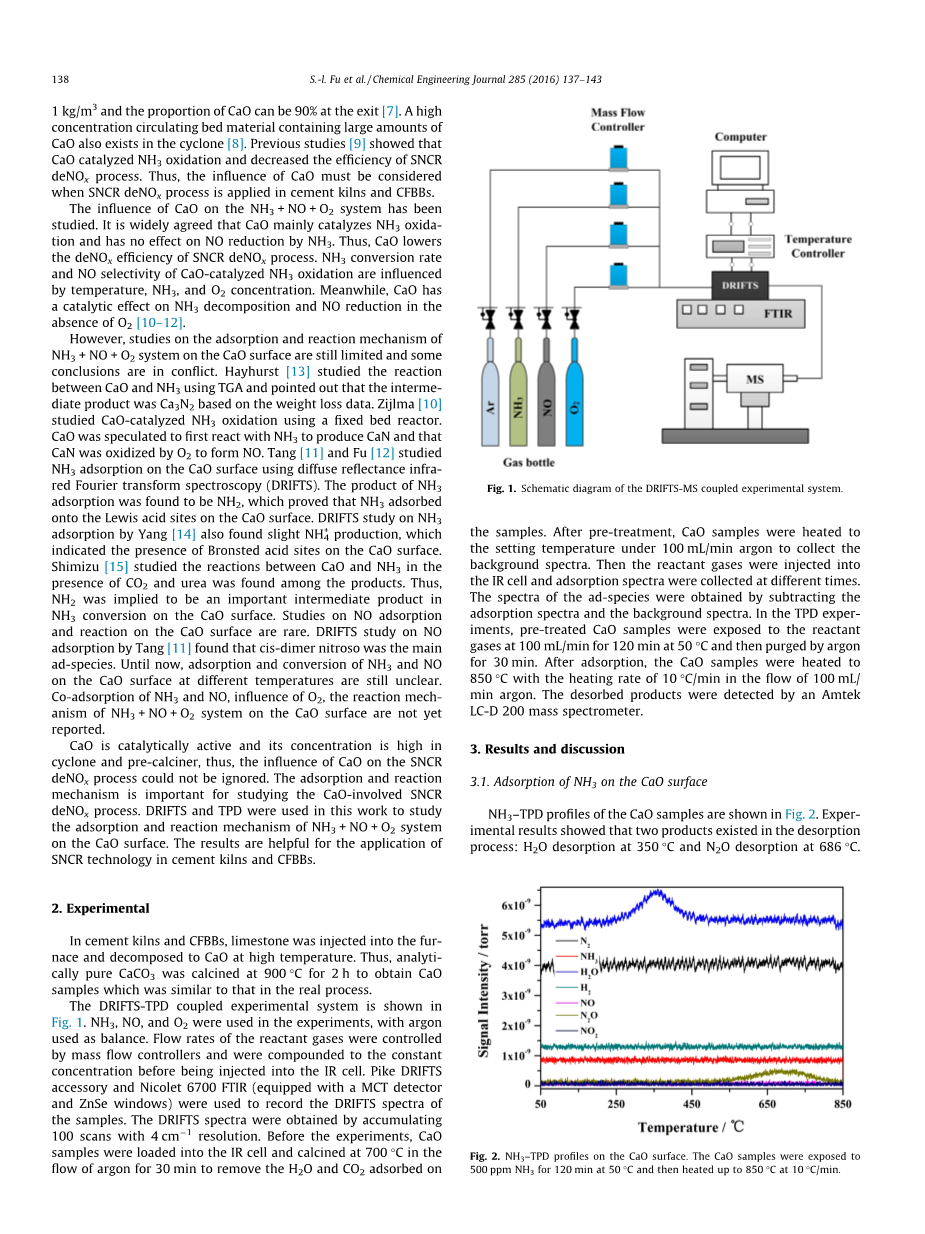
DRIFTS-TPD耦合实验系统如图所示图。1.在实验中使用NH3,NO和O2 ,使用氩作为余量。通过质量流量控制器控制反应气体的流速,并在注入IR池之前将其混合至恒定浓度。Pike DRIFTS附件和Nicolet 6700 FTIR(配备MCT检测器和ZnSe窗口)用于记录样品的DRIFTS光谱。通过以4cm—1 分辨率累积100次扫描获得DRIFTS光谱。在实验之前,将CaO样品加载到IR池中并在700℃下在氩气流中煅烧30分钟以除去吸附在其上的H2O和CO2样品。预处理后,将CaO样品加热至100mL / min氩气下的设定温度,收集背景光谱。然后将反应气体注入IR池中,并在不同时间收集吸附光谱。通过减去吸附光谱和背景光谱获得ad物质的光谱。在TPD经验中
将预处理的CaO样品以100mL / min的速率在50℃下暴露于反应气体120分钟,然后用氩气吹扫30分钟。吸附后,将CaO样品以100℃/分钟的氩气流速以10℃/分钟的加热速率加热至850℃。解吸的产品由AmtekLC-D 200质谱仪检测。
3.结果和讨论
3.1.NH3 在CaO表面的吸附
CaO样品的NH3-TPD曲线显示在图2.实验结果表明,在解吸过程中存在两种产物:H2O在350℃解吸,N2O解吸在686℃。在加热过程中未观察到NH3 解吸,这表明NH3 在CaO表面上的物理吸收较弱。H2O解析显示NH3 吸附后发生夺氢。产生的氢原子
与晶格氧反应生成H2O并在350℃下解吸。N2O解析显示NH3 解离产生的氮原子与晶格氧反应形成N2O并在686℃解吸。NH3 在CaO表面上的DRIFTS光谱不同
温度显示在图3.在100°C,NH3后观察到866,1377,1528和3000-3700 cm—1 的吸附带
吸附。866,1377和1528厘米—1 的波段可归因于吸附在路易斯酸位点的NH2 自由基的伸缩振动[14,16–22].可以将3000-3700cm—1 的带分配给OH自由基的振动。[14,23].NH3 吸附在路易斯和布朗斯台德酸位点上分别形成NH2 和NH 自由基。在DRIFTS光谱上仅观察到NH2 条带,这证明NH3 仅吸附在CaO表面上的路易斯酸位点上。杨(Yang)观察到NH 吸附在布朗斯台德酸位上[14] 可能与样品的未完成预处理有关。已知布朗斯台德酸位点在高温下容易被破坏。煅烧炉和旋风分离器预先的温度约为900°C,CaO来自石灰石的煅烧。因此,Bronsted酸位点几乎不存在。同时,拉米斯的研究[19] 还表明,NH3 吸附后可能产生NH2 和NH 。但是只有NH2 具有反应性。在200℃时,NH3 的吸附和解离速率增加,并且强度增加。在300°C时,NH2 解离和OH解吸增加,NH2 和OH带的强度变弱 -TPD个人资料图2 还表明在该温度范围内开始H2O解吸。在400℃时,很难观察到NH2 和OH的带,这意味着氢的取代
完成NH2 和OH解析。然而,在2176cm处观察到强带—1 ,其可被指定为双倍
氮键[24].NH3 ad-种类在400℃下的光谱表明二氮化物是在NH3 解吸过程中产生的。NH2 脱氢后,在2176 cm—1 的二氮化物带甚至在500°C时增强,这意味着可能产生二硝化物来自两个氮原子的二聚化。雷米斯[19] 表明NH2 可能二聚成N2H4;因此,二硝基氮也可以由N2H4的夺氢产生。NH3-TPD实验表明,NH3 中的氮以N2O的解析解吸。因此,N2O是二氮化物与晶格氧之间反应的产物。
3.2.在CaO表面上吸附NO
CaO样品的NO-TPD曲线显示在图4.实验结果表明,在解吸过程中存在两种产物:在360℃下解吸NO,在686℃下解吸N2O。没有在360°C下解吸是由于NO化学吸附在CaO表面。在吸附后发现NO转化为硝酸盐在金属氧化物上[25–27].唐[11] 发现在NO吸附在CaO表面后形成硝基。因此,推测硝基或硝酸盐是NO吸附的产物。而CaO表面。随着温度的升高,硝基或硝酸盐在682℃时作为N2O分解和解吸。TPD实验表明,吸附的NO在CaO表面部分还原为N2O,这表明CaO的氧化能力弱于NO。在不同温度下CaO表面上NO ad-物种的DRIFTS光谱显示在100°C下的NO后,观察到1256,1345,1519和3000-3700 cm—1 的吸附带吸附。可以将1256和1519cm处的条带—1 分配给单齿硝酸盐[25–31] 并且可以将1345cm处的条带—1 指定为顺式 - 二聚体亚硝基[32].可以将3000-3700 cm—1 的波段分配给OH振动[23].OH基团由CaO表面上残留的痕量水形成。NO吸附后,形成NOH基团[28,33],这增强了OH波段的强度。由于CaO表面的OH在高温下容易被破坏,因此在3000-3700 cm—1 处的ATURE带强度随着回火的增加而迅速降低 -。随着温度升高到200-300°C,仍然存在观测到的在1256和1519厘米—1 硝酸盐的条带。然而,1345cm—1 的顺式二聚体亚硝基带消失了。NO-TPD实验表明,该温度范围内解析物为NO。因此,顺式二聚体亚硝基是解吸NO前提体。随着温度
增加到400-500°C,只有1502的单齿硝酸盐带[25,26],1332和1084厘米—1 [28] 观察到了。就这样在NO-TPD实验解析吸的N2O是由高温下单齿硝酸盐的分解产生的。DRIFTS光谱证明NO吸附在CaO表面并形成单齿硝酸盐和顺式二聚体亚硝基。随着温度的升高,顺式二聚体亚硝基和单齿硝酸盐分别分解为NO和N2O。
3.3.NH3 和NO在CaO表面上的共吸附
NH3 的TPD曲线和CaO表面的NO共吸附示于图6.在解吸中观察到四种产物。
过程:H2O在350℃解吸,在360℃解吸NO,在360℃解吸N2 ,在686℃解吸N2O。与NH3 和NO的TPD曲线相比,在360℃下观察到的解析产物N2。如图所示图3和5,NH3 解离NH2 和顺式二聚体亚硝基在此温度范围下分解为NO-。因此,N2 的解吸表明NH2 可以与NO反应在CaO表面上产生N2 ,如式(1)所示。(1).ad物种NH3 与NO之间的反应也证明NH3 与CaO催化的NO之间的反应遵Langmuir-Hinshelwood机理。
NH2eth;adTHORN; thorn; NOeth;adTHORN; ! N2 thorn; H2O eth;1THORN;
在100和500℃下,NH3 和NO在CaO表面上的共吸附中的ad-species的DRIFTS光谱显示在图7,与单次吸附NH3 和NO相比。在100°C时,NH2 在1528 cm—1,单齿硝酸盐在1510和1256 cm—1,在NH3 和NO共吸附的光谱中观察到在1345cm处的顺式二聚体亚硝基—1和在3000-3700cm处的OH—1 。实验结果表明,NH3 和NO可以同时吸附在CaO表面,并且ad-species与它们的相似吸附。在500℃时,仅在光谱中观察到1502,1332和1084cm处的单齿硝酸盐带—1 ,类似于NO单吸附。同时,没有观察到tride。这是因为二氮化物NH2的前体在与NO的反应中被消耗,这抑制了二硝化物的产生。中的现象图7 再次证明了NH2 和NO之间的反应(如式(1)所示。(1)并且反应遵循Langmuir-Hinshelwood机制。
3.4.O2 对NH3 和NO的ad-种类的影响
在100和500℃下,O2 对CaO表面上NH3 ad物种的影响显示于图8.在100℃下在光谱中观察到NH2 在866,1377和1528cm—1 处的谱带(图8(a))CaO暴露于NH3后。OH的范围在3000-范围内还观察到3700cm—1 。一旦样品暴露于O2,NH2 和OH的条带在延长的时间内显着增强。NH3 首先吸附在CaO表面上,然后吸附的NH3 离解成NH2。暴露于O2后,增强的NH2 条带强度表明O2 促进NH3 向NH2的解离。NH3 离解成NH2 是CaO表面NH3 转化的速率控制步骤[11,12];因此,O2 增加了NH3的转化率,如式(1)所示。(2).在500°C(图8(b)),在CaO暴露于NH3后,观察到2176cm处的二硝化物带—1 。例子然后将其暴露于O2 ,并且随着时间的延长,二硝酸酯带的强度迅速减弱。由于在CaO表面上仅存在二氮化物和O2 ,因此二氮化物带的弱化证明在NH2 解离中产生的二硝化物化合物可被O2氧化,如式(1)所示。(3).
NH3eth;adTHORN; thorn; O2eth;adTHORN; ! NH2eth;adTHORN; thorn; OHeth;adTHORN; eth;2THORN;
- Neth;adTHORN; thorn; O2eth;adTHORN; ! 2NO eth;3THORN;
- 在100和500℃下,O2 对CaO表面上的NO ad-种类的影响显示在图9.在暴露于O2后,CaO表面上的NO ad-种类的条带随着时间增加而不变。实验结果表明,O2 对NO ad物种没有影响。结果还解释了CaO对NO氧化没有催化作用的现象。
3.5.NH3,NO和O2 在CaO表面上的反应
在500℃的CaO表面上NH3 和NO之间的反应中的ad-物种的DRIFTS光谱显示在图10.暴露于NO 30分钟后,单齿硝酸盐带于1332
资料编号:[4159]
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。
您可能感兴趣的文章
- 两种水处理厂活性污泥生物群落生物指示物真核生物的比较:一个案例研究外文翻译资料
- 针叶凋落物挥发性有机化合物的顶空-固相微萃取技术分析外文翻译资料
- 流动注射-在线固相萃取化学发光系统测定天然水中痕量铜外文翻译资料
- 电感耦合等离子体原子发射光谱法,火焰原子吸收光谱法和紫外 – 可见分光光度法测定制革废水中的总铬外文翻译资料
- 表面改性对活性炭吸附苯酚和2,4-二硝基苯酚的影响外文翻译资料
- 伊斯坦布尔一级和三级城市污水处理厂的成本比较评价外文翻译资料
- 基质固相分散(MSPD)是测定粉尘中多溴二苯醚(PBDEs)的简单有效的样品制备技术外文翻译资料
- 乙酰胆碱酯酶是广谱有机环境污染物的潜在生物标志物外文翻译资料
- 纳米材料导论概述:广谱应用外文翻译资料
- 植物和粪便生物炭的性质及其对邻苯二甲酸二丁酯和菲的吸附外文翻译资料