
英语原文共 8 页,剩余内容已隐藏,支付完成后下载完整资料
一个可以响应pH/H2O2然后分离纳米载体调节肿瘤缺氧进行有效联合治疗的智能型白蛋白-MnO2纳米颗粒
Qian Chen, Liangzhu Feng, Jingjing Liu, Wenwen Zhu, Ziliang Dong, Yifan Wu, and Zhuang Liu
随着人类对肿瘤生物学认识的不断进步,目前普遍认为肿瘤是一个结构相当复杂、具有独特肿瘤微环境 (tumor microenvi-ronment,TME) 的异常器官。对于一个实体肿瘤来说,除了肿瘤细胞,还有很多其他类型的细胞如成纤维细胞、巨噬细胞和各类免疫细胞,它们被凝结的细胞外基质包围,并由结构不均匀的肿瘤血管供养。因此,这种复杂的肿瘤结构拥有许多生物载体,这些生物载体可以用于癌症治疗中抗癌治疗药物的递送。就纳米医学而言,已知纳米颗粒大小通常在控制其在肿瘤中的滞留和渗透中发挥重要作用。一般而言,大尺寸 50-100 nm 的纳米颗粒通过增强渗透性和滞留 (EPR) 效应来延长其在血液循环的滞留时间,保持有效的肿瘤蓄积量。然而,肿瘤相关性成纤维细胞和致密的细胞外基质将是大尺寸纳米颗粒深层间质渗透的主要障碍。另一方面,尺寸在 10 nm 以下的纳米颗粒具有更好的瘤内穿透效率,但可能降低 EPR 效应。由此提出,理想的纳米药物颗粒在血液循环过程中应相对较大 (50-100 nm),以达到有效的 EPR 来源的肿瘤聚集量,但纳米药物颗粒一旦进入肿瘤内部,应足够小以增强其穿透力。
另一方面,癌细胞的快速生长以及扭曲的肿瘤血管会导致实体瘤内部氧气供应不足以及酸化。众所周知,缺氧和 pH 值呈酸性(TME 的共同特征)不仅会促进肿瘤血管生成和转移,还会导致治疗抵抗和治疗失败。 特别是对于某些类型的氧气参与细胞杀伤过程的疗法如放疗和光动力疗法 (PDT),TME 中缺氧会导致肿瘤治疗无效。 最近,各种策略已被探索以克服缺氧,包括使用人工血液替代品(如氟化碳)将氧气运输到肿瘤中, 或在肿瘤内部用催化剂在合适的地方生成氧气,这些策略都有显示了提高 PDT 疗效的可喜结果。尽管如此,开发对 TME 敏感的智能治疗型纳米药物以获得更好的瘤内间质扩散,同时可以调节 TEM(如缓解缺氧)以获得更好的治疗效果将是非常有意义的。
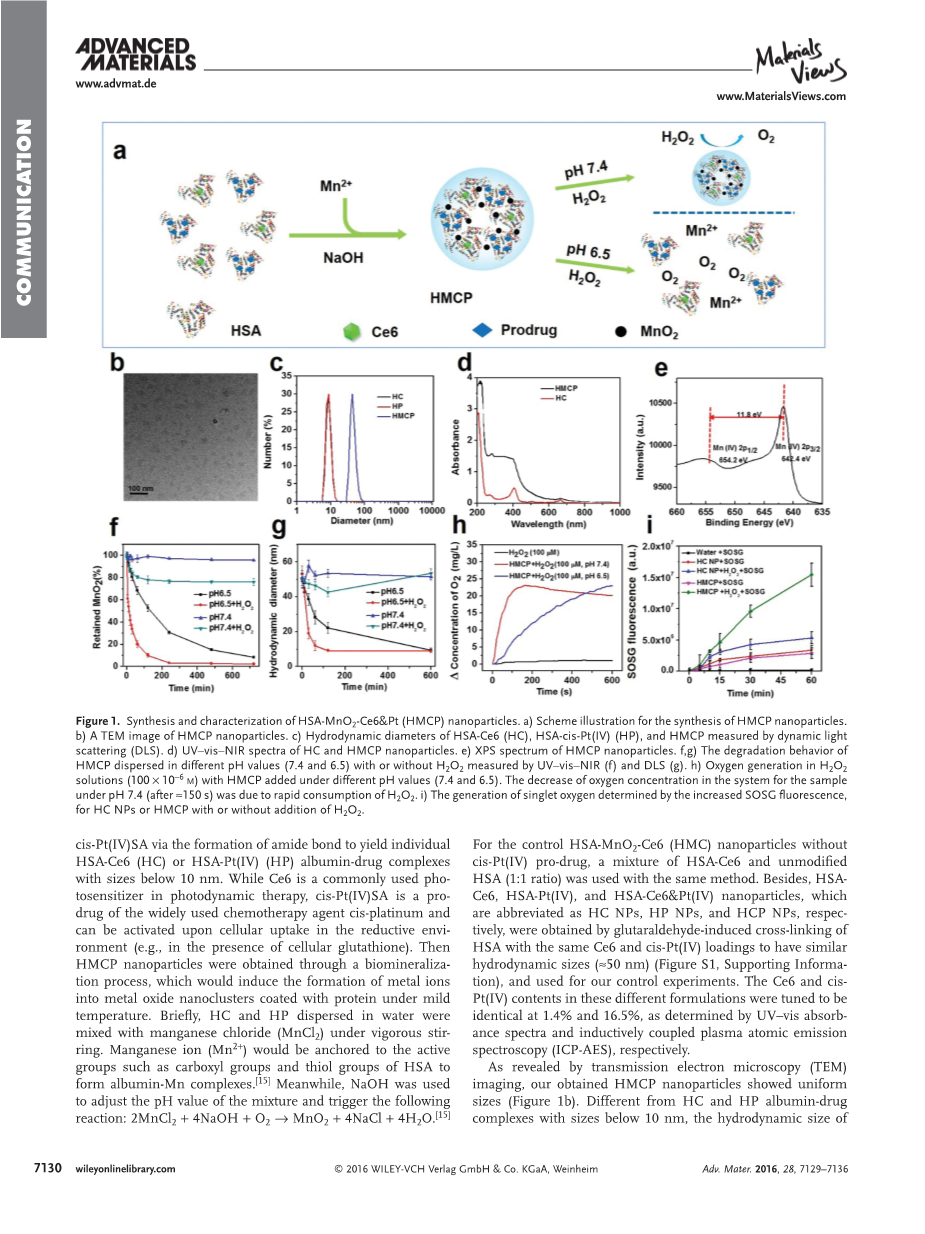
图一. HSA-MnO2-Ce6amp;Pt (HMCP) 纳米粒子的合成和表征。a)合成 HMCP 纳米颗粒的示意图。b)HMCP 纳米颗粒的 TEM 图像。c)HSA-Ce6 (HC)、HSA-cis-Pt (IV) (HP) 的流体力学直径,和动态光散射 (DLS) 法测定的 HMCP。d)HC 和 HMCP 纳米颗粒的紫外-可见-近红外光谱。e)HMCP 纳米颗粒的 XPS 光谱。f,g)用紫外-可见-近红外 (f) 和 DLS (g) 测定了分散在不同 pH 值(7.4 和 6.5)、有或无 H2O2 条件下 HMCP 的降解行为。h)在不同 pH 值(7.4 和 6.5)下加入 HMCP 的 H2O2 溶液(100times;10-6 M)中生成氧气。pH 7.4(约150 s 后)下样品系统中氧浓度的降低是由于 H2O2的快速消耗。i)对于添加或不添加 H2O2 的 HC NPs 或 HMCP,通过增加的 SOSG 荧光测定单线态氧的生成。
作为最丰富的血浆蛋白和一种通用的生物相容性给药载体,人血清白蛋白 (Human serum albumin,HSA)得到了广泛的探索,它能够在碱性条件下通过生物矿化将无机离子隔离,形成蛋白包被的金属氧化物纳米团簇。因为已知二氧化锰 (MnO2) 纳米颗粒对 H2O2具有高反应性,会产生 O2,并会在酸性 pH 下分解, 本课题组基于白蛋白的 Mn2 生物矿化,设计了多功能的智能型pH/ H2O2响应的 HSA 包被MnO2 纳米颗粒。在该体系中,以光敏剂氯 e6 (Ce6) 或 c,t,c-[Pt(NH3)2-(O2CCH2CH2COOH)(OH) Cl2] (cis-Pt(IV)SA) 作为顺铂的前体药物对 HSA 进行预修饰,然后将HSA作为模板和包被分子,在碱性条件下通过生物矿化诱导 MnO2 纳米团簇的形成,获得多组分 HSA-MnO2-Ce6amp;Pt (HMCP) 纳米颗粒。 利用 MnO2 敏感的 pH/ H2O2 响应行为,这类 HMCP 纳米颗粒一方面能够通过与肿瘤内部内源性 H2O2 反应在合适的位置生成 O2,从而有希望克服肿瘤与缺氧有关的PDT抗性。 另一方面,在酸性 TME 中的 HMCP 纳米颗粒将逐渐降解为小尺寸 (lt; 10 nm) 的单个治疗性白蛋白-药物复合物,其出肿瘤内渗透性大大增强,将进一步改善光动力和化疗联合治疗的结果。因此,这项研究提出了一个有趣的纳米级药物递送系统的概念,它不仅揭示了纳米药物响应 TME后为了增强肿瘤内扩散的尺寸变化,而且能够调节不受欢迎的 TME,为改善癌症治疗创造更好的条件。合成 HMCP 纳米颗粒的方法如图 1a 所示。
HSA 首先通过形成酰胺键与 Ce6 或 cis-Pt (IV) SA 预偶联,生成大小低于 10 nm 的单个 HSA-Ce6 (HC) 或 HSA-Pt (IV) (HP) 白蛋白-药物复合物。虽然 Ce6 是光动力疗法中常用的光敏剂,但 cis-Pt (IV) SA 是广泛使用的化疗药物顺铂的前体药物,可在还原性环境中被细胞摄取时激活(例如,在细胞存在谷胱甘肽的情况下)。然后通过生物矿化工艺得到 HMCP 纳米粒子,在温和的温度下诱导金属离子形成包覆蛋白质的金属氧化物纳米团簇。简言之,在剧烈搅拌下,将分散在水中的 HC 和 HP 与氯化锰 (MnCl2) 混合。锰离子 (Mn2) 会固定在 HSA 的羧基、巯基等活性基团上,形成白蛋白-Mn 配合物。同时,使用 NaOH 调节混合物的 pH 值,并触发以下反应:2MnCl2 4NaOH O2 MnO2 4NaCl 4H2O。为了对照不含 cis-Pt (IV) 前体药物的HSA-MnO2-Ce6 (HMC) 纳米粒,本课题组采用同样的方法对HSA-Ce6和未修改的HSA(1:1比率)的混合物进行实验。此外,HSA-Ce6、HSA-Pt (IV) 和 HSA-Ce6amp;Pt (IV) 纳米颗粒(分别缩写为 HC NPs、HP NPs 和 HCP NPs,通过戊二醛诱导的 HSA 交联获得, Ce6 和 cis-Pt (IV) 负载相同,具有相似的流体力学尺寸 (约50 nm)(图 S1,支持信息)),也用于本课题组的对照实验。通过紫外可见吸收光谱法和电感耦合等离子体原子发射光谱法 (ICP-AES) 测定,将这些不同处方中的 Ce6 和顺铂 (IV) 含量调整至相同,分别为 1.4% 和 16.5%。
透射电子显微镜 (TEM) 成像显示,本课题组获得的 HMCP 纳米颗粒大小均匀(图 1b)。与尺寸小于10nm的HC和HP白蛋白药物复合物不同,HMCP的流体动力学尺寸测量约为50nm(图1c),表明所形成的MnO2纳米团簇被多个白蛋白包裹在单个纳米颗粒中。其次,测定了HC和HMCP的紫外-可见-近红外吸收光谱。与HC相比,HMCP在300-400nm处出现了一个新的吸收带,这可能归因于MnO2的表面等离子体子带(图1d)。X射线光电子能谱(XPS)也用于研究形成的HMCP中锰元素的化学状态(图1e)。观察到两个分别位于MnO2的Mn(IV)2p1 / 2和Mn(IV)2p3 / 2自旋轨道峰的特征峰在654.2和642.4 eV,这进一步证明了MnO2的成功形成。
众所周知,实体肿瘤内部癌细胞的旺盛代谢和血液供应不足,不仅会导致TME酸化,还会导致肿瘤内部H2O2含量显着升高。考虑到MnO2与H2O2和H 的反应性,因此,本课题组仔细研究了HMCP纳米颗粒在不同介质中MnO2 的降解行为(图S2,支持信息)。 MnO2的去辐射可以通过其特征吸收带的减小来确定(图1f)。发现在pH 6.5时,HMCP中MnO2的吸光度迅速下降,特别是在H2O2存在下,这可以进一步促进MnO2的分解。相反,在不存在H2O2的情况下,HMCP中的MnO2在pH 7.4下显得相当稳定。即使添加了H2O2,在中性pH下12 h后,HMCP样品中仍保留着asymp;80%的MnO2。酸诱导的H2O2促进的MnO2降解可以通过以下反应解释:
MnO2 2H Mn2 H2O 1/2O2
MnO2 H2O2 2H Mn2 2H2O H
然后本课题组研究人员想了解酸度诱导的MnO2分解是否会诱导HMCP分解成基于单独白蛋白的复合物。因此测量了分散在不同溶液中的HMCP纳米颗粒的流体动力学尺寸。发现在pH 6.5下,HMCP纳米颗粒将缓慢解离,导致粒度随时间的减小。值得注意的是,在此pH值下存在H2O2时,这些纳米颗粒的离解显著加快,并且几乎所有HMCP纳米颗粒在此条件下2小时内都会分解成游离白蛋白。相反,即使在添加H2O2的情况下,分散在中性pH 7.4下的HMCP纳米颗粒的流体动力学尺寸也没有显着变化,表明HMCP纳米颗粒在中性环境中相当稳定(图1 g)。
已知在中性条件下,MnO2能够起催化剂的作用,诱导H2O2分解产生O2。 尽管在弱酸性条件下,MnO2仍在充当催化剂,但会与H2O2和H反应生成O2和水溶性Mn2离子。因此,在不同pH值(6.5和7.4)下加入HMCP时,在H2O2溶液中生成的O2用氧气探针(JPBJ-608便携式溶解氧计,上海雷克斯仪器厂)进行了测量。正如预期的那样,尽管在pH 7.4下由HMCP触发的氧气生成速度在大约100 g / min的条件下,HMCP在两个pH值下均含有100times;10 -6 M H2O2的溶液中产生了大量的O2(图1 h)。较之于pH 6.5更快,这可能是由于MnO2在较高pH下对H2O2分解具有更高的催化活性。然而,加入HMCP后,在H2O2溶液(pH 6.5,1times;10 -3 M)中仍观察到大量的氧气气泡,生动地说明了MnO2强烈诱导H2O2分解的能力(图S3,支持信息)。
在PDT过程中,光敏剂在光照下会将基态(三重态)的氧气转化为细胞毒性单线态氧气(1O2),从而杀死癌细胞。考虑到在HMCP存在下从H2O2产生有效的O2,本课题组研究人员想了解在TME相关浓度的H2O2存在下Ce6缀合的HMCP是否是一种优异的PDT试剂。因此,本课题组测量了在光照射(660 nm,5 mW cm2)下,HMCP和HC NPs产生1O2的情况,后者是通过戊二醛交联的HC纳米颗粒(尺寸约为50 nm,与HMCP相似)。将溶液的pH调节至6.5times;106,并添加100times;106 M H2O2以模拟TME。单重态氧传感器绿色(SOSG),其淬灭荧光将在1O2存在的情况下恢复,用于1O2测量。不出所料,在没有H2O2的情况下,HMCP和HC NPs都显示出相似的1O2生成效率。有趣的是,由于MnO2触发了H2O2产生的O2,因此在H2O2存在下,HMCP显着增加了1O2的产生,而HCP的1O2产生的增加却少得多。加入H2O2观察到HC NP(图1 i)。因此,在与肿瘤内部微环境有关的条件下,在H2O2存在下,使用光敏剂偶联的MnO2基纳米颗粒,可以显着提高PDT的效率。
然后研究了不同纳米颗粒的细胞吸收效率和体外治疗效果。首先,将鼠乳腺癌4T1细胞与HMC,HC NP和具有相同Ce6浓度的游离Ce6孵育不同的时间。共聚焦荧光成像和流式细胞术结果均显示,在与HMC和HC NPs孵育的4T1细胞中强Ce6荧光,而用游离Ce6处理的细胞由于其较低的细胞吸收效率而显示出较弱的Ce6荧光(图2 a,b)。接下来,本课题组通过将它们与一系列浓度的4T1细胞培养48小时,测试了各种顺铂制剂(包括游离顺铂,HP NP和HMCP)的体外癌细胞杀伤功效。已发现,所有这三种顺铂制剂均显示出对4T1细胞相似的细胞毒性,这表明这些纳米颗粒中的顺铂前药仍然有效杀死癌细胞(图2c)。
<s
剩余内容已隐藏,支付完成后下载完整资料</s
资料编号:[245857],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 用于神经胶质瘤SPECT成像的一种新型东亚钳蝎氯毒素衍生物外文翻译资料
- 基于聚乙烯亚胺的诊疗性纳米平台用于靶向胶质瘤单光子发 射计算机断层扫描成像和抗癌药物传递外文翻译资料
- 用于体内肿瘤靶向抗癌药物输送的多功能聚乙烯亚胺基纳 米平台外文翻译资料
- 一种细菌可激活的纳米探针治疗耐甲氧西林金黄色葡 萄球菌感染的研究外文翻译资料
- 特异性聚合物抗菌剂对病原体具有显著的膜破坏和光动力损伤,可 以抑制高机会致病性细菌外文翻译资料
- 关于骨肉瘤的诊断、治疗和治疗策略的综述外文翻译资料
- 代谢组学结合通路分析表征BED-3诱导的小鼠生殖毒性反应的代谢变化外文翻译资料
- 转录组分析证实金丝桃素的抗肿瘤机制 HOS胶质母细胞瘤细胞系的研究外文翻译资料
- 非靶向血浆代谢组学分析精液异常男性不育症外文翻译资料
- 热反应和蛋白酶-可分解干扰素-多肽共轭物通过时间空间程序两步释放动力学对于肿瘤的治疗外文翻译资料


