药用植物中活性化合物的生产:
从植物组织培养到生物合成
摘 要:在过去数十年中, 植物组织培养已成为一种替代植物的完整种植在生产宝贵的次生代谢物。人参和紫锥菊紫癜的不定根培养达到了 1minus;10的规模。转基因技术和遗传稳定性等分子生物学技术在植物组织培养研究中得到越来越广泛的应用。诱导的研究已深入到诱导机制中, 包括信号分子、功能基因等。越来越多的生物诱导, 如尼日尔和酵母, 用于增加植物组织培养中的活性化合物。我们还讨论了合成生物学在青蒿素、紫杉醇和丹参生物合成研究中的应用。药用植物活性成分在生物合成的研究中为实现大量生产活性成分提供了前所未有的可能性。植物组织培养能产生活性。
关键词:生物合成;功能基因;药用植物组织培养;次生代谢产物
- 序言
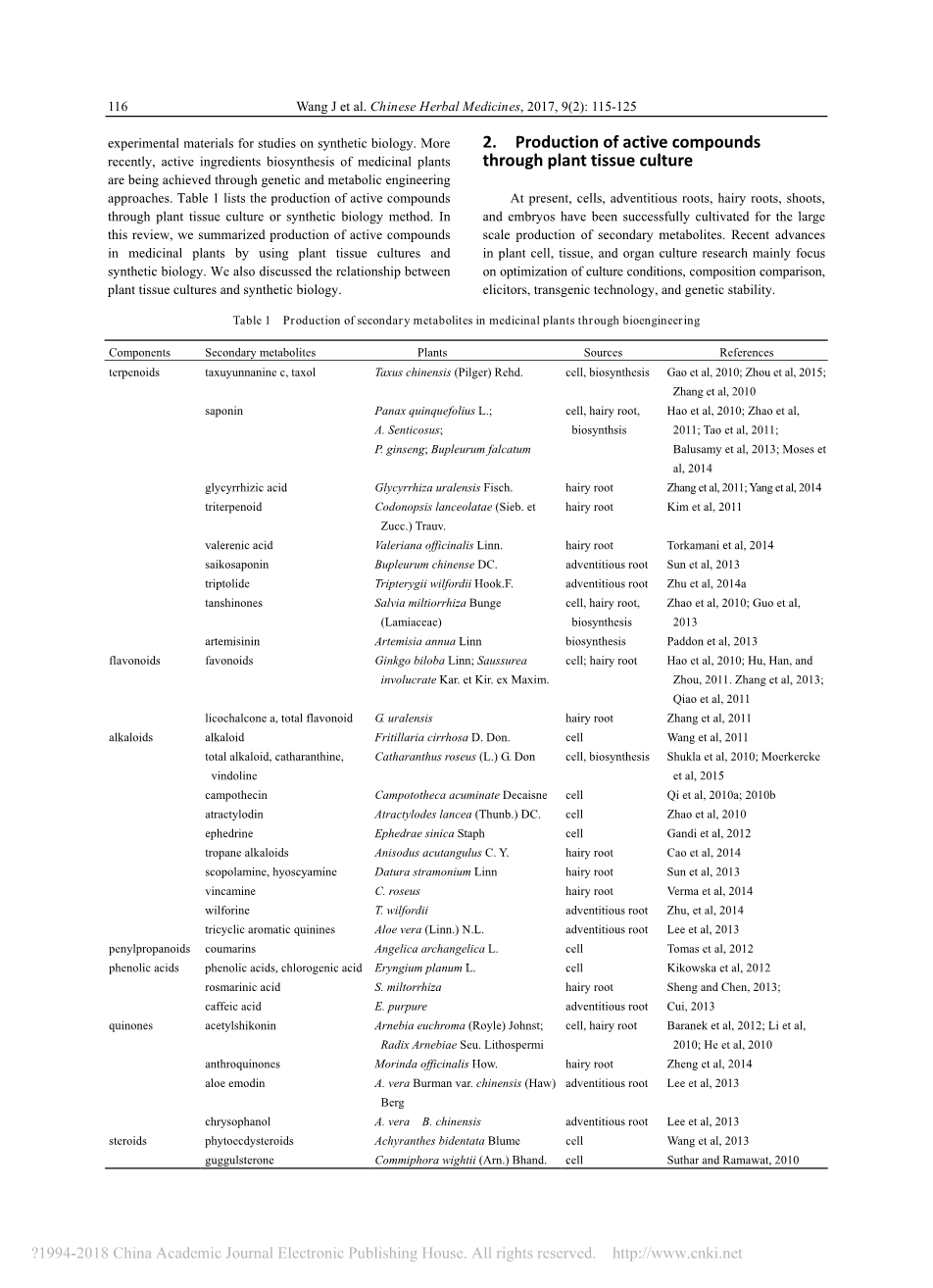
最近几十年里,在合成生物学的研究中,植物细胞、组织、器官已经作为完整的植物种植的实验材料的替代品而出现。最近, 药用植物的活性成分生物合成是通过遗传和代谢工程方法来实现的。表1列出了通过植物组织培养或合成生物学方法生产活性化合物。在本文中,我们利用植物组织培养和合成生物学方法对药用植物中活性化合物的生产进行总结。我们还讨论了植物组织培养与合成生物学的关系。
- 植物组织培养生产活性化合物的研究
目前, 细胞、不定根、毛根、芽、胚等均已成功培养成次生代谢产物的规模化生产。植物细胞、组织和器官培养研究的最新进展主要集中在培养条件优化、成分比较、诱导、转基因技术和遗传稳定性等方面。
2.1培养条件的优化
在药用植物组织培养过程中, 一些影响组织生长的理化因素和次生代谢产物的靶的合成, 如温度、光、pH、电、磁、电磁辐射、机械力、超声波, 介质类型, 介质盐强度, 接种密度, 碳源, 氮源, 以及在培养基中的一些微量金属离子。
一般情况下, 培养温度为 20minus;28 ℃, 培养基 pH 值5.6minus;6.0。通常情况下, 蔗糖是最好的碳源, 因为它具有热不稳定的性质,在加压蒸馏后大部分会分解为 D-葡萄糖和 D-果糖后蒸压, 只有一小部分的蔗糖留下, 这是更有利于吸收和利用。除了提供在介质中需要的碳骨架和能量, 在一定程度上, 碳源可以调节介质中的渗透压力。NAA、IBA、2,4-D和 BA 是最常见的荷尔蒙。在人参的组织培养中, 人们发现IBA适合于侧根的诱导和生长 (Jeong等, 2009), 而2,4-D适合于愈伤组织诱导 (Mercedes等 2002)。无机氮, 例如, 培养基中的硝酸盐 (NO3minus;) 和铵 (NH4 ) 以供应硝酸盐或铵盐。硝酸盐和氨氮水平的相对比例对细胞分裂和培养分化有重要影响。Sivakumar的实验结果表明, 培养基中铵态的氮比较低, 更有利于人参皂苷的合成 (Sivakumar Sivakumar, 2005)。张等人也报告说, 培养基中氮含量的降低更有利于多糖的合成 (张 et, 1996)。
2.2不同组织培养中化学成分的比较
近年来, 不同组织培养中的化学成分日益受到研究, 包括培养体系、细胞系、植物器官、培养模式和诱导。
举例来说, Chavan (2014) 用 LC-质谱法比较了供体、DSO 和 ISO 衍生叶中酚类物质的含量, 结果表明在所鉴定的化合物中成分均相似。在太子参太子参 (益智)Hoffm。以不定根培养、电喷雾电离串联质谱 (ESI–MSn) 分析方法比较了不定根 (AR) 与已有根的活性化学成分, 结果表明, pseudostellarins A、C、D 和 G 均来自于AR(王等 al, 2015)。此外, 在甘草不定根培养中, ESI-MS 分析表明, 在水杨酸中发现了两种新的黄酮类化合物包括(3R)-vestitol 和 glycyrol (Li et, 2015)。
2.3
由于药用植物中次生代谢产物含量较低, 一些活性化合物难以分离。因此, 研究者试图通过诱导植物细胞中特定基因的表达, 来增加植物次生代谢物的产生。李 (2013) 研究了水杨酸、甲基茉莉、乙烯对维拉不定根次生代谢产物积累的影响。结果表明: 用水杨酸处理不定根时, 芦荟大黄素和大黄酚的含量显著增加, 可产生37种化合物。
2.4转基因技术
植物转基因技术是一种诱导生物体遗传性状变异的方法, 在整合后转化为寄主植物的外源基因而表达。用某些转基因的植株可以显著改善植物的相应特征, 产生高水平的活性化合物或高生物量的植物。农杆菌介导不仅是首次应用于植物的转基因方法, 而且是植物转化使用最广泛的方法。在植物组织培养中, 植物转基因技术主要应用于毛根培养和悬浮细胞的建立。
由Ri 质粒转化的毛状根生长迅速, 含有完整的代谢通路的表达, 为药用植物次生代谢产物的工业化生产提供了广阔的前景。此外, 毛状根为新的药物筛选提供了大量的植物材料, 因此生物转化可以产生许多新的化合物。目前, 人参皂甙和小檗碱已获得了毛根培养的商业化生产 (Kim et al, 2011)。
在对山葡萄细胞培养 (Aleynova et, 2015) 的研究中, 调查了CDPK 的多基因家族 (VaCPK9、VaCPK13、VaCPK21 和 VaCPK29)的过度表达对其白藜芦醇积累和生长参数的影响。结果表明, VaCPK29 的过度表达可以增加在四个独立转化的 V. amurensis型细胞系中的白藜芦醇含量和新鲜生物量的积累,使其比空矢转化的愈伤组织更多。此外, C. roseus中的色氨酸脱羧酶 (strictosidine) 和长春基因在 Echeveria setosa V.集成细胞悬浮液中成功地过度表达。 (Priyanka et al, 2015)
2.5遗传稳定性
植物组织培养是植物快速传质的潜在工具, 具有控制次生代谢物生产的巨大潜力。然而, 由于再生植物体细胞变异而导致的隐性遗传缺陷的发生, 会严重限制该系统的优越性。因此, 必须建立组织培养苗的遗传均匀性, 以保证苗种的品质, 使其具有商业价值。有几种策略可用于检测这些变异包括简单序列重复 (ISSR) PCR, 随机扩增多态性 DNA (RAPD) 和流式细胞术。
ISSRs 被应用于特定基因的物种, 以调查在种内水平的变异性。随机扩增多态 DNA (RAPD) 方法是一种基于 PCR 技术, 在低退火条件下, 利用任意核苷酸序列的单个短引物, 放大随机 DNA 片段。该技术已广泛应用于物种分类、遗传图谱和系统发育 。在试管苗 Ceropegia santapaui 的研究中, 用 ISSR 和 RAPD 比较了直接梢器官 (DSO) 衍生苗、间接射出器官 (ISO) 衍生苗和母植株之间的遗传稳定性。采用RAPD 和 ISSR 两种方法发现 DSO 源苗的基因和和其母株十分的相似, 异源苗的 ISSR 变异性很低 (Chavan et, 2014)。流式细胞术在细胞培养中的应用包括以下三方面: (1) 细胞程序性死亡 (凋亡) 的流式细胞仪分析与检测。该技术具有良好的精确度和速度。黄(2014) 研究了荧光显微镜和流式细胞仪在线粒体悬浮细胞活性及其生理效应方面的应用, 并检测了悬浮细胞的程序化死亡率; (2) 应用流式细胞仪对细胞周期动力学进行研究, 并探讨生长阶段与靶代谢物含量之间可能的相关性。Stancheva (2011) 研究了悬浮细胞周期动力学的流式细胞仪分析。结果表明, G0/G1 和 S 相的细胞比例在培养过程中差异不显著 (69%–76% 和9%–13% 之间), 而 G2/M-phase 细胞的比例一直增加到第八天, 指数细胞生长阶段结束。(3) 应用流式细胞仪对染色体倍数进行分析。Heide开发了一种新的细胞计数方法, 结合细胞染色和自动共焦荧光显微镜。这种方法首次允许了我们确定植物细胞悬浮培养的细胞特定的生产力 (Heide, 2014)。
近年来, 细胞、不定根、毛根、芽、胚等均已成功培养成次生代谢产物的规模化生产。例如, 人参的不定根已达到 10 kL (Jeong et al、2014) 和叶连翘不定根达到500L (Murthy et, 2014), 紫锥菊紫癜的不定根 (Linn)加杨雄达到1000L(Murthy et, 2014), Acanthopanax senticosus的多倍体细胞胚的培养(Rupr.Maxim)Haems达到500L(Paek et al, 2014)。一些分子生物学技术在植物组织培养研究中得到越来越多的应用。然而, 植物组织培养商业化的例子还很少。
3.
尽管已经努力了四年的时间,但是植物组织培养技术生产植物次生代谢物仍面临着许多生物和生物技术的限制。其中主要的障碍之一是植物组织培养中植物次生代谢物的产量很低。诱导包括各种来源的化学物质或生物因子,能有效防御目标生物的系统 (赵, 2005)。由于植物次生代谢物的主要作用是保护植物免受生物和非物质的胁迫, 诱导可以引起植物中一系列的防御反应, 包括在完整的植物中或者在细胞培养中积累一系列植物防御性次生代谢物。因此, 利用该方法可以提高植物次生代谢产物的产量。
3.1诱导信号转导
诱导可被位于等离子膜或膜表面的植物受体识别。受体被激活, 然后反过来激活其效应器, 如离子通道, GTP 结合蛋白 (G 蛋白), 蛋白激酶和氧化爆裂。活化效应能促进信号分子 (水杨酸、茉莉酸、一氧化氮等) 的合成, 将诱导信号转移到下游基因上, 进一步放大诱导信号, 使次生代谢产物。
3.1.1活性氧种类 (ROS)
ROS 的产生是植物细胞应用于诱导治疗的反应 (Zhao, 2005)。有一个即时的细胞反应触发植物防御信号, 增加活性氧的积累, 如过氧化氢 (H2O2), 超氧化物阴离子 (O2minus;) 和羟基自由基 (bull;OH)。ROS 对植物的防御反应会产生各种影响, 包括防御性基因活化以及防御性复合诱导。植物抗氧化防御系统可以通过增加抗氧化酶的活性 (He et, 2010) 来清除 ROS。植物抗氧化防御系统可以通过增加抗氧化酶的活性, 如超氧化物歧化酶 (SOD)、过氧化氢酶 (CAT) 和抗坏血酸过氧化物酶来清除活性氧。在红豆杉细胞培养过程中, 随着枯萎病菌粗提取物的加入, SOD、POD、CAT 的酶的活性发生了较大变化, 产生了大量的 ROS;紫杉醇含量为控制量的四倍。
虽然 ROS 诱导调节代谢产物的机制我们还尚不清楚, 但作为信号分子的 ROS的增加, 可以调解植物细胞壁的加厚, 细胞死亡, 过敏反应, 以及防御基因的表达,这是诱导代谢反应的关键信号 (Wang et al, 2015)。
3.1.2一氧化氮(NO)
NO 是一种生物活性分子, 在动物和植物细胞 (Beligni 和 Lamattina, 2000) 中可以发挥出多种不同的信号功能。NO可以在植物中产生由光介导的非酶的类胡萝卜素的NO2, 或硝酸盐硝酸的酶 (Neill et, 2002)。研究表明, NO是植物细胞死亡的标志, 防御基因的表达, 在氧化爆裂和茉莉酸的合成中起着关键作用。人参悬浮液的培养过程中, 随着无供体硝普钠的加入, 氧化酶的活性增加, H2O2被诱导(Hu et al,2003).Xu (2005) 发现, 从Aspergillum niger的细胞壁的诱导出的了 H. 贯叶细胞的多种反应, 包括 NO 生成、茉莉酸生物合成和桃生产。但是, NO合成酶抑制剂能有效抑制诱导诱导的茉莉酸生物合成。
3.1.3 Ca2
[Ca2 ] 细胞色素从胞外和细胞内来源的峰值也是诱导诱发的早期反应, 它可以调节几乎所有下游诱导诱发的反应 (Rahimi, 2015)。这种大量的诱导的 [Ca2 ] 细胞色素的峰值可以直接调节所有防御基因的表达或激活许多细胞内与Ca2 有关的反应, 如钙调素, 可以进一步激活 Ca2 /calmodulin-dependent 蛋白激酶,膜束缚酶或转录因子。例如, (P) H 氧化酶, 一种主要来源于的 ROS 生产 (如 O2和H2O2) 是由 [Ca2 ] 细胞色素的的峰值诱导。这些 ROS, 蛋白激酶叶栅, 和脂质信号信使可以进一步转移和放大诱导信号的下游反应
3.1.4 JA和SA
多不饱和脂肪酸可以产生信号, 如 oxylipins, 包括 JA, MJ, 和JA代谢物 (Wasternack, 2007)。长期以来, JA 及其相关化合物都是许多植物次生产物生物合成的综合信号, 是诱导信号的传感器或中介, 导致植物次生代谢产物的积累。研究表明, JA 诱导特定的酶催化生化反应, 以生产低分子量的防御化合物, 例如, 在植物中的多酚, 生物碱, quinines, 萜, 肽。
水杨酸是一种信号分子, 通常可以在植物中发现其有非常低的浓度。在植物组织培养系统中, 水杨酸作为诱导的应用已被大量报道。这种化合物的产生及其对次生代谢产物生物合成的机理与植物防御系统密切相关。在真菌诱导治疗过程中, SA 迅速积聚在感染部位, 并传播到植物的其他部位, 诱导广泛的防御反应, 并诱导基因表达相关的生物合成和生产的一些类次生植物中的代谢产物。
3.2诱导分类
在诱导的基础上, 可分为生物型和非诱导型两种。
3.2.1生物诱导
生物诱导有来自病原体或微生物细胞的生物学起源, 即真菌、细菌、病毒和其他微生物代谢物, 特别是碳水化合物或多糖组分, 可用于诱发或刺激植物细胞和组织培养中次生代谢产物的产生 。在 Taverniera cuneifolia (Roth) 的根的培养, 活微生物培养中,五真菌和五株细菌被用作诱导, 以改善甘草酸含量。结果表明, Mucor hiemalis 染色可诱导最大量4.90 毫克/克的甘草酸。在细菌诱导中, 根瘤菌根瘤菌
全文共10031字,剩余内容已隐藏,支付完成后下载完整资料

英语原文共 11 页,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[12726],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 选择性能量转移催化烯烃的含硼几何异构化外文翻译资料
- 瑞德西韦阻滞SARS-CoV-2聚合酶的作用机理外文翻译资料
- 铱催化的共轭二烯的C-H烯基的烯丙基化反应外文翻译资料
- 铱和布朗斯特酸协同催化烯丙醇对萘酚衍生物的对映选择性脱芳构化外文翻译资料
- 新型选择性MT2受体配体2-(苯硫基)苯并[b]噻吩类化合物的制备和药理学评价外文翻译资料
- Ilimaquinone是一种海绵代谢产物,通过gadd153介导的途径发挥抗癌作用外文翻译资料
- 用环境敏感药物释放的三氧化二砷靶向介孔二氧 化硅纳米颗粒有效治疗三阴性乳腺癌外文翻译资料
- 复方中草药对雄性荷斯坦犊牛生长表现,胴体特征和肉质的 影响外文翻译资料
- 线粒体在没有人体ATP合酶的亚基c时渗透性转 变的持久性外文翻译资料
- 基于呋喃类化合物构建环氧树脂 2,5-呋喃羧酸(FDCA)生物基环氧树脂的合成及性能研究外文翻译资料


