
英语原文共 9 页
纳米粒子介导的药物递送的最新进展
Bipul Kumar,Kanika Jalodia,Pradeep Kumar,Hemant K. Gautam
摘要
对控制药物输送的引入寻求开发合适的药物载体可以将足够剂量的药物传递给患病的病变部位。已经测试了各种药物递送中的载体,如纳米结构,包括脂质,聚合物,树枝状大分子和磁性纳米颗粒。纳米颗粒通过提供小粒径的药物可以改善在水中难溶的药物的递送,允许在血流中更快地溶解,从而使靶向以细胞或组织特异性方式递送药物。 本文概述了纳米粒子在药物输送中的制备和使用的最新进展。
内容
1.简介 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 261
1.1.药物输送系统中的纳米载体. . . . . . . . . . . . . . . . . . . . . . . . . . .262
1.2.药物掺入纳米颗粒的制备. . . . . . . . . . . . . . . . . . . . . . . . . . . . .262
1.3.预制聚合物的分散. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 262
1.4.溶剂蒸发法 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 262
1.5.自发乳化或溶剂扩散法. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .262
1.6.聚合方法 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 262
1.7.凝聚或离子凝胶化方法. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .263
1.8.使用超临界流体技术生产纳米颗粒 . . . . . . . . . . . . . . . . . . . . . 263
1.9.自组装纳米粒子 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .264
1.10.静电纺丝法 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .264
1.11.影响纳米颗粒介导的药物递送的参数 . . . . . . . . . . . . . . . . . .264
1.11.1粒径 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 264
1.11.2纳米粒子的表面性质 . . . . . . . . . . . . . . . . . . . . . . . . . . .264
1.11.3药物装载 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 265
1.11.4药物释放 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 265
1.12.纳米粒子在疾病中的作用 . . . . . . . . . . . . . . . . . . . . . . . . . . . . 265
1.12.1纳米粒子检测和治疗肾脏疾病 . . . . . . . . . . . . . . . . . . .265
1.12.2纳米粒子给药系统在结核病化疗中的应用 . . . . . . . . 265
1.12.3纳米粒子用于改善皮肤病药物的局部应用 . . . . . . . . 265
1.12.4纳米粒子靶向传染病的药物 . . . . . . . . . . . . . . . . . . . . .266
1.12.5纳米粒子在阿尔茨海默病中的应用 . . . . . . . . . . . . . . .266
1.12.6纳米粒子包含各种抗癌剂 . . . . . . . . . . . . . . . . . . . . . . .266
1.13.纳米粒子的临床试验 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .266
2.总结
致谢 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 266
参考文献 . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 266
- 简介
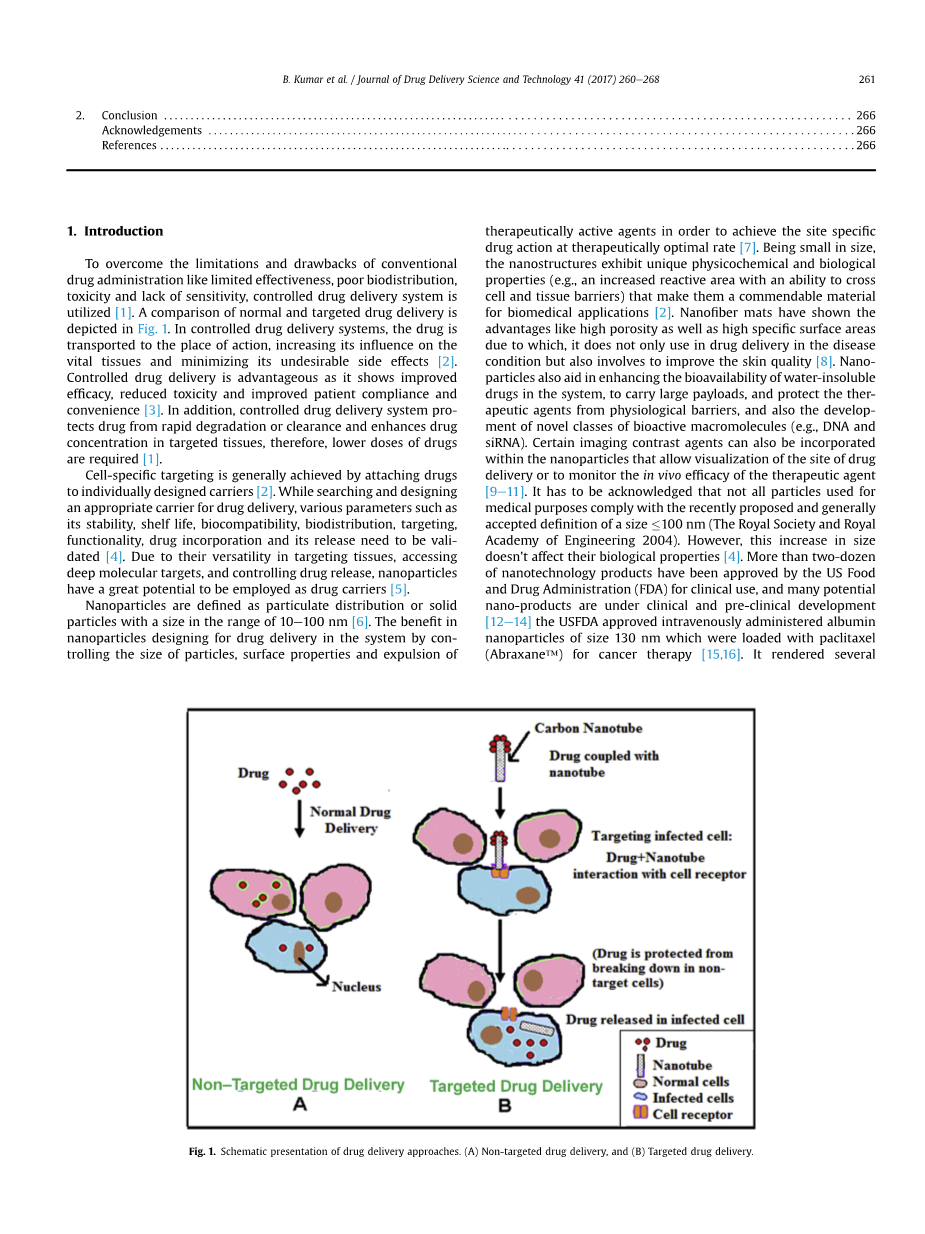
为了克服了传统给药系统的局限和弊端,如效力有限,生物分布差,毒性大和缺乏敏感性,控制给药系统是一种选择[1]。正常给药和靶向给药的比较如图1所示。在控制给药系统中,药物被运到起作用的地方,增加了它对病变组织的影响作用,并尽量减少了其不良副作用[2]。药物受控递送是有利的,因为它显示出改善功效,降低毒性和改善患者依从性的优点[3]。此外,受控药物输送系统可保护药物免于快速降解或清除,并提高靶组织中的药物浓度,从而降低必需的药物剂量[1]。
细胞特异性靶向通常通过将药物附着在单独设计的载体上来实现[2]。在搜索和设计时,适用于药物输送的载体的各种参数如其稳定性,保质期,生物相容性,生物分布,靶向,功能,药物掺入能力及其释放需要验证[4]。由于它们有在靶向组织的多功能性,访问深层分子靶能力和控制药物释放能力,纳米粒子有很大的潜力被用作药物载体[5]。
纳米颗粒定义为颗粒分布或固体尺寸在10-100 nm范围内的颗粒[6]。纳米粒子在设计用于系统中药物递送时的益处,是通过控制粒子的大小,表面性质和治疗活性剂的排出以实现特定位点上药物作用在治疗上的最佳速率[7]。纳米结构体积小,具有独特的物理化学和生物学特性(例如,具有增加的反应区域且能够穿过细胞和组织屏障)使它们成为值得称道的用于生物医学应用的材料[2]。纳米纤维垫已经显示出来了高孔隙率和高比表面积等优点。因此,它不仅用于疾病的药物输送,还涉及改善皮肤质量[8]。纳米颗粒还有助于增强系统中水不溶性药物的生物利用度,携带大的有效负载,保护治疗剂免受生理屏障,以及开发新型生物活性大分子(例如DNA和siRNA)。还可以掺入某些成像造影剂在纳米颗粒内,从而显示药物的位置递送或监测治疗剂的体内功效[9-11]。必须承认的是,并非所有用于医学目的的颗粒都符合最近提出的并且普遍接受的尺寸小于等于100nm的定义(英国皇家学会和皇家工程学院2004)。然而,这种尺寸的增加并不影响它们的生物学特性[4]。超过二十多种纳米技术产品已获得美国食品和药物管理局(FDA)批准用于临床,许多潜在的纳米产品正在用于临床和临床前开发[12-14] USFDA批准静脉注射尺寸为130纳米的白蛋白的纳米颗粒,其载有紫杉醇(Abraxane TM)用于癌症治疗[15-16]。与传统的药物递送相比,它具有几个优点,包括消除毒性,因为cremophor是一种先前在配方中使用的溶剂,并且由于可以施用和递送的药物剂量增加而具有更好的功效[5]。
-
- 药物输送系统中的纳米载体
具有独特物理化学和生物学特性的纳米载体比大分子更容易被细胞包吞; 因此,它们可以有效地用作目前可用的生物活性化合物的递送工具[17]。纳米载体用于医疗应用必须是生物相容的(能够与生物系统整合而不引起免疫反应或任何疾病效果)和无毒(对给定的生物系统无害)[2]。使用纳米颗粒作为药物递送系统的突出特征包括容易操纵颗粒大小及其表面特征以实现主动和被动药物靶向,在运输过程中在目标部位控制和持续排出药物,增加药物的治疗效果功效和减少副作用,高载药量,使用包括肠胃外,眼内,口腔,鼻腔等在内的各种给药途径,避免聚结,使稳定性增强,给药药物分子的流动性降低,以减少药物渗漏[18]。 设计和制备纳米载体时要考虑的特性总结在图2中。
理想地,由天然或合成聚合物制备的纳米颗粒是廉价的,无毒的,可生物降解的,非血栓形成的,非免疫原性的,非炎性的,粒径lt;100nm并且抑制血小板聚集[18]。
-
- 药物掺入纳米颗粒的制备
纳米颗粒可以由不同类型的材料制备,例如蛋白质,多糖和合成聚合物(表1)。基质的选择取决于许多因素,包括必需的纳米粒子大小,药物的基本性质,如溶解度,稳定性,表面特征(电荷和渗透性),生物降解程度,生物相容性和毒性,所需的药物输送特性,最终产品的抗原性。主要用于制备纳米颗粒的方法是亲水聚合物的离子凝胶化或凝聚,单体聚合和预形成的聚合物[7,18]。然而,其他方法如超临界流体技术和非润湿模板中的颗粒复制(PRINT)也用于制备纳米颗粒。自组装和静电纺丝方法也已用于增强纳米颗粒的稳定性和有效性。非润湿模板中的颗粒复制可绝对控制颗粒大小,形状和组成,这对于工业中纳米颗粒的大规模生产来说是一个巨大的突破[28,29](见表2)。
-
- 预制聚合物的分散
该技术用于从聚(氰基丙烯酸酯)(PCA),聚(D,L-乙交酯),PLG制备可生物降解的纳米颗粒;聚(D,L-丙交酯 - 共 - 乙交酯)(PLGA)和聚(乳酸)(PLA),可以通过以下各种方式实现:
-
- 溶剂蒸发法
该方法可用于制备生物相容性和可生物降解的微米和纳米粒子,并且它提高了药物材料的生物利用度,有效性和溶出速率[30]。 将聚合物和疏水性药物溶于有机溶剂如氯仿,二氯甲烷和乙酸乙酯中。 该聚合物 - 药物含水混合物的乳化通过使用表面活性剂或乳化剂进行,所述表面活性剂或乳化剂形成各种类型的乳液,例如水包油(o / w),w / o / w,s / o / w,o / o / w和o / o等乳液[31,32]。 通过减压或不断搅拌除去所用的有机溶剂。 纳米结构的粒径取决于所用稳定剂的类型和浓度,聚合物的浓度和超声波处理;通过这种方法可以生产出更小的颗粒[30]。
-
- 自发乳化或溶剂扩散法
该方法是溶剂蒸发方法的略微改进。在该方法中,使用含有机溶剂的水溶性溶剂作为油相。由于溶剂的自发扩散,在两个不混溶相之间产生界面湍流。这导致颗粒的形成。为了产生更小的颗粒,使用增加浓度的极性溶剂[33]。
-
- 聚合方法
该方法使用聚合的单体亚单元在水溶液中形成纳米颗粒。 一旦聚合完成,药物在聚合期间被包封在纳米颗粒中或者被吸附在纳米颗粒的表面上。 然后通过在等渗介质中超速离心或再悬浮颗粒,从纳米颗粒分散体系中除去用于聚合的各种稳定剂和表面活性剂。 通过该技术,已经生产了几种纳米颗粒,如聚氰基丙烯酸丁酯或聚(烷基氰基丙烯酸酯)纳米颗粒。 纳米胶囊的形成及其粒径取决于所用表面活性剂和稳定剂的类型和浓度[6-33]。
-
- 凝聚或离子凝胶化方法
大多数研究旨在使用亲水性可生物降解聚合物(如海藻酸钠,壳聚糖和明胶)制备纳米颗粒。Calvo P等人,1997年[34]开发了利用凝聚法从壳聚糖构建亲水性纳米粒子的方法。 该方法需要混合聚合物壳聚糖,二嵌段共聚物环氧乙烷或环氧丙烷(PEOPPO)和聚阴离子三聚磷酸钠,两者都占混合物的两个水相。在该混合物中,壳聚糖的阳离子氨基酸被静电吸引到阴离子三聚磷酸盐上以形成凝聚层。由此形成的凝聚层在纳米范围内。另一方面,室温下的离子凝胶化由于离子相互作用条件,材料从液体转变为凝胶。
-
- 使用超临界流体技术生产纳米颗粒
使用常规方法如溶剂萃取 - 蒸发,溶剂扩散和有机相分离方法制备纳米颗粒的缺点是它们使用有机溶剂。如此形成的纳米颗粒对环境无害;它们有毒,不适合用于生物系统。或者,超临界流体技术旨在制备可生物降解的微米和纳米颗粒,因为超临界流体对环境是安全的。超临界流体是一种溶剂,无论压力如何,它都保持在高于其临界温度的单相中。最常用的超临界溶剂之一是超临界CO2。其广泛使用的特性是其温和的临界条件(Tc = 31.1℃,Pc = 73.8巴),不易燃,无毒且价格低廉。超临界反溶剂和关键溶液的快速膨胀是最广泛的超临界技术。超临界反溶剂的方法需要溶解溶剂,使其在液体溶剂中微粉化,例如甲醇,可用超临界流体均化。由于溶质不溶于
资料编号:[5372]
以上是毕业论文外文翻译,课题毕业论文、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。
您可能感兴趣的文章
- 选择性能量转移催化烯烃的含硼几何异构化外文翻译资料
- 瑞德西韦阻滞SARS-CoV-2聚合酶的作用机理外文翻译资料
- 铱催化的共轭二烯的C-H烯基的烯丙基化反应外文翻译资料
- 铱和布朗斯特酸协同催化烯丙醇对萘酚衍生物的对映选择性脱芳构化外文翻译资料
- 新型选择性MT2受体配体2-(苯硫基)苯并[b]噻吩类化合物的制备和药理学评价外文翻译资料
- Ilimaquinone是一种海绵代谢产物,通过gadd153介导的途径发挥抗癌作用外文翻译资料
- 用环境敏感药物释放的三氧化二砷靶向介孔二氧 化硅纳米颗粒有效治疗三阴性乳腺癌外文翻译资料
- 复方中草药对雄性荷斯坦犊牛生长表现,胴体特征和肉质的 影响外文翻译资料
- 线粒体在没有人体ATP合酶的亚基c时渗透性转 变的持久性外文翻译资料
- 基于呋喃类化合物构建环氧树脂 2,5-呋喃羧酸(FDCA)生物基环氧树脂的合成及性能研究外文翻译资料


