摘要
本文研究的是以脂肪酸作为捕收剂的萤石浮选中由于沉淀物的形成及其与矿物表面的相互作用引起的复杂行为。在本文中以棕榈酸作为一种典型的羧酸捕收剂来进行实验,采用了几种不同的实验测试方法来描述实验中水溶液的行为及棕榈酸和棕榈酸钙盐的沉淀以及它们对萤石润湿性和浮选行为的影响。
1介绍
化学吸附是由于被吸附物和吸附剂之间形成了化学键,因此吸附剂在被吸附物表面形成了单层覆盖。在含水矿物体系中被称为“化学吸附”的许多过程可能是晶格离子的化学交换的表面反应,该反应可持续至其中一种反应物被消耗完或反应达到平衡。在浮选中可以找到很多的例子,例如在金属阳离子活化硫化矿过程中,会与晶格离子发生交换反应,又如在氧化铅矿物的硫化过程中会发生阴离子的交换反应。在加入少量试剂量和较短的反应时间的条件下,这种体系中可以很明显的观察到单层覆盖的情况。
微溶盐矿物的浮选如磷灰石,方解石和萤石似乎受与羧酸捕收剂的化学相互作用影响。众多研究人员对油酸捕收剂作用于盐型矿物反应的结果进行了红外光谱测试,结果表明生成的金属—羧酸盐键来源于化学吸附化学交换或化学反应。在较低的pH条件下,也发现了一些物理吸附的现象。然而,在这种类型的体系下,研究人员发现捕收剂的吸附程度通常远远超出单层,并且在实际上可能在是在表面形成了新的皂相,这意味着捕收剂作用的过程应该被认为是一种表面反应而不是作为一种吸附过程。事实上,Kitchener(1984)写道:“皂化的主要问题是确定产物的结构,在这种情况下,它似乎不太符合简单的单层模型。在假设这种体系的“吸附等温线”是通过沉淀曲线得到的前提下,含钙矿物将继续存在并与油酸钠几乎无限地反应下去hellip;hellip;.
经过详细的研究,M.C.Fuerstenau和Elgilanni(1966)认为,用长链磺酸盐和油酸盐捕收剂浮选钙活化石英会产生大量的钙沉淀。Laskowski等人 (1989)详细介绍了他们研究弱电解质捕收剂的结果,特别强调了胺沉淀在石英浮选上的作用。2003年,Fa等人的研究表明油酸钙的胶体颗粒凝结在萤石表面并使其易于浮动。
本研究的目的是描述典型脂肪酸的溶液化学、其沉淀物的界面行为以及它们对萤石浮选行为的影响。尽管还用肉豆蔻酸和油酸(其在酸性pH下作为液滴存在)进行了广泛的研究,但本文仅讨论了棕榈酸/萤石体系。
2材料和方法
本研究中使用的脂肪酸纯度为99%以上,并且无机化学品都是试剂级。所有实验用水均为三次蒸馏水。萤石晶体在瓷研钵中粉碎以制备75times;147和147times;300mu;m大小的式样。把样品通过高梯度磁力分离器以除去少量弱磁性矿物,然后除湿,并用稀硝酸洗涤以除去方解石污染物。洗涤后,将样品干燥并储存以备后续实验。
实验中使用的仪器:用玻璃/甘汞电极进行pH测量,精度为0.05pH单位。使用Birtcher浊度计来测量浊度和用Malvern Zetasizer测量胶体材料的粒度。用Zeta-Meter来测量电泳迁移率(用于确定zeta;电位)。通过原子吸收分光光度法测定金属离子的浓度,并使用UIC Coulometer通过碳分析测量有机物的浓度。用300毫升改良的Hallimond试管进行浮选试验,试样用4g的147times;300微米大小的萤石样品。在所有实验中,使用KNO3建立0.01M的最小离子强度,但在Ca2 浓度很高时要过量添加。接触角通过气泡附着样品抛光表面测量。
3实验结果与讨论
3.1棕榈酸水溶液
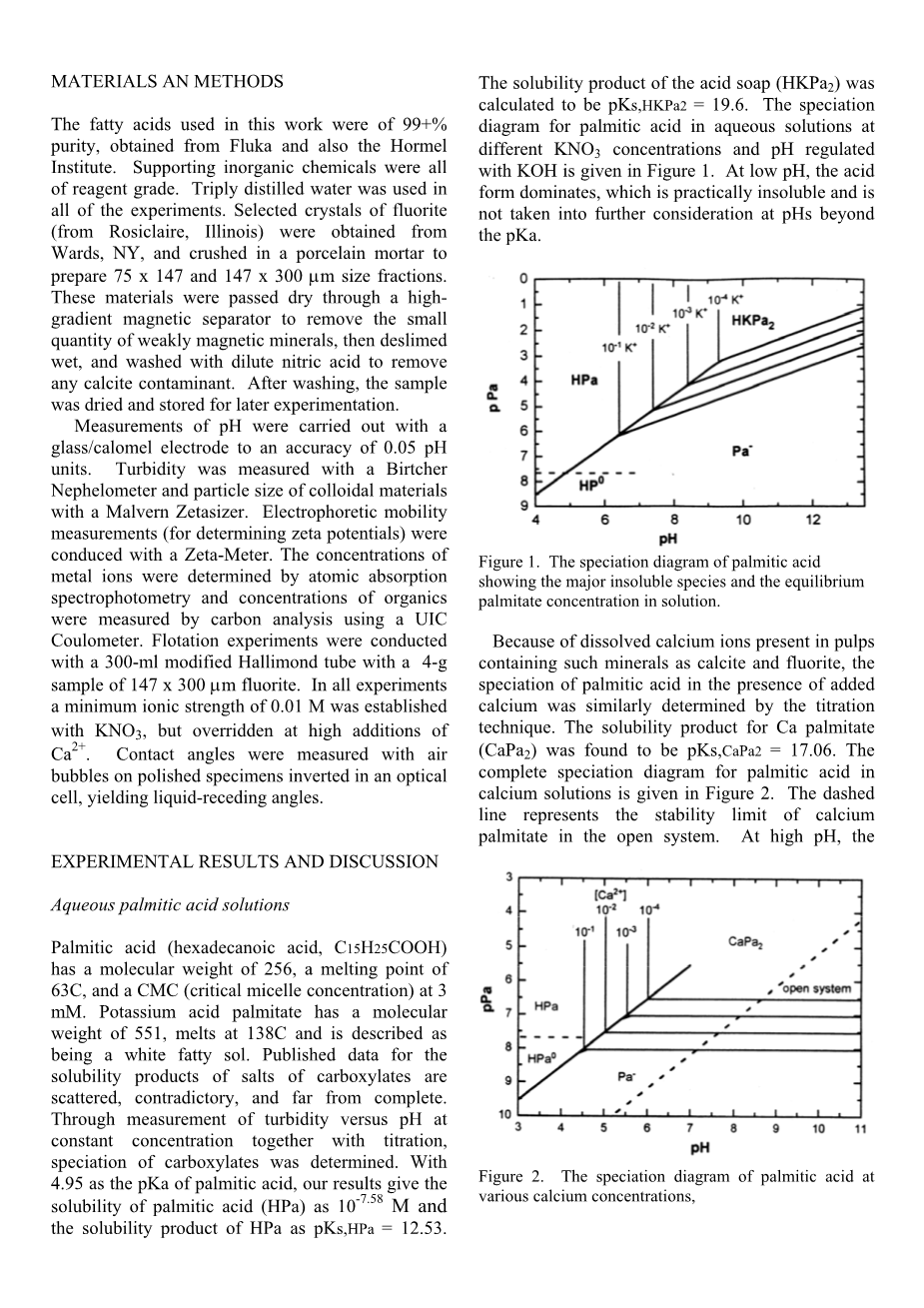
棕榈酸(十六烷酸,C15H25COOH)分子量为256,熔点为63℃,CMC(临界胶束浓度)为3mM。酸式棕榈酸钾的分子量为551,在138℃熔化为白色脂肪溶胶。已有的羧酸盐盐溶解度产物的数据是分散的,相互矛盾的,也是不完全的。本实验通过在恒定浓度和滴定下测量浊度和pH值,从而测定羧酸盐的形态。取pKa为4.95的棕榈酸,测量结果表明棕榈酸(HPa)的溶解度为10-7.58M,HPa的溶度积为pKs.HPa=12.53。酸皂(HKPa2)的溶度积计算为pKs.HKPa2 = 19.6。图1给出了用KOH调节不同KNO3浓度和pH值的水溶液中棕榈酸的形态图。在低pH的条件下,酸形式占主导地位,也是不溶的,并且在pKa以外的pH不再进一步考虑。
图1.棕榈酸的形态图,显示溶液中主要不溶物和平衡棕榈酸酯浓度
由于在含有方解石和萤石等矿物的矿浆中存在溶解的钙离子,所以在添加钙的情况下棕榈酸的形态只能通过滴定技术来确定。发现棕榈酸钙(CaPa2)的溶度积为pKs.CaPa2 = 17.06。图2给出了棕榈酸在钙溶液中的完整形态图。虚线代表开放系统中棕榈酸钙的稳定极限。 在高pH值时,碳酸盐浓度增加并最终以方解石沉淀。方解石的溶度积是pKs.CaCO3 = 8.23,萤石的溶度积pKs.CaF2 = 10.3。
图2.各种钙浓度下棕榈酸的形态图
在已经发表的许多棕榈种类的产物溶解度资料中,我们的结果与DuReitz(1975)的结果是相匹配,他的结果也是在开放系统中采用与萤石达到平衡的棕榈酸脂肪酸研究得到的,并且结果呈现在图3中。矿物/试剂在浮选条件下的相互作用通常不会达到平衡,但图1~3中给出的结果为解释萤石与棕榈酸的浮选行为提供了手段。
PH
图3.在开放系统中与萤石平衡的含水棕榈酸物质的稳定域
3.2棕榈酸盐沉淀物的Zeta电位
通过微电泳,将棕榈酸颗粒的zeta;电位(zeta;)看作为pH的函数。将含有10-3M棕榈酸酯的储备溶液稀释至10-4M,并将pH降至低于沉淀边缘的期望值。平衡30分钟后测量颗粒的迁移率以计算zeta;电位。图4显示了棕榈酸的zeta;电位与pH的函数关系。HPa颗粒的zeta;电位随着pH增加变得越来越负的最可能的解释是棕榈酸根离子的吸附。在我们的工作中,在更酸性pH值下的zeta;电位未被确定,但Laskowski等人(1989)发现月桂酸和肉豆蔻酸颗粒在pH值在3和3.5之间时带正电荷,该正电荷必须由氢离子的吸附产生。因为与萤石平衡的水溶液含有10-4M Ca2 ,所以需要确定不同浓度的钙溶液中沉淀的棕榈酸物质的zeta;电位,结果也在图4中。在低pH下,曲线与棕榈酸基础曲线一致,但在的不同pH值下急剧平稳,这是由钙离子的浓度造成的。图上显示的HPa和CaPa2稳定域之间的边界非常接近钙沉淀的zeta;电位偏离棕榈酸的zeta;电位的点。
图4.不同钙水平下棕榈酸酯类物质的zeta;电位与pH值的关系。 在较低pH下,颗粒是棕榈酸和棕榈酸钙,箭头表示HPa / CaPa2的边界
在整个pH范围内,CaPa2颗粒上边界处的酸的zeta;电势被保留。这可能是由于带负电荷的棕榈酸根离子的吸附引起的,并且在沉淀之后,它们与钙盐平衡的浓度由可溶性产物决定。
3.3棕榈酸对萤石Zeta电位的影响
通过电泳评估在0.1mM添加的硝酸钙存在下萤石的zeta;电位是pH的函数。图5给出的结果表明,zeta;电位在pH 10.7时反转,与Miller和Hiskey(1972)的早期发现一致。在很大的pH范围内,10-5M棕榈酸酯的添加对zeta;具有显着的影响,如图5中给出的结果所示。在pH=3左右时,zeta;电位开始明显偏离不加棕榈酸酯的曲线,在pH=4左右时逆转符号并在pH=6左右时达到最小值,这代表棕榈酸钙形成的条件。随着pH值进一步升高,zeta;变得不太负,在pH=8.7时再次反转符号,并在pH=9.5左右时重新合并萤石曲线。Fuerstenau和Shibata(1999)讨论了如何通过添加表面活性剂来改变代表特定吸附自由能的zeta;电位(Delta;zeta;)。当Delta;zeta;为零(曲线重合)时,没有特定的吸附。 因此,矿物的浮选应该发生在添加了表面活性剂的曲线与没有添加捕收剂曲线相偏离的pH区域。
在标准化学吸附系统中,吸附剂反转其表面电荷后,具有和不具有特定吸附剂的曲线总是再次聚集在一起。如果阴离子捕收剂是特定的,那么随着pH升高,矿物表面变得带负电后,两条曲线再次结合。在目前的情况下,当矿物表面仍带正电荷时,两条曲线会聚到一起。这表明棕榈酸盐/萤石相互作用是带电荷的棕榈酸和棕榈酸钙颗粒与萤石发生多相凝聚而不是吸附,或者CaPa2不如Pa-离子稳定。
图5.在含有0.1mM钙的水溶液中含有和不含棕榈酸的萤石的zeta;电位
3.4萤石上的棕榈酸酯吸附
由于捕收剂在矿物表面上的吸附通常被认为是浮选的先决条件,因此测量捕收剂吸附量是有益的。为此目的,将已知表面积的萤石样品加入到pH=6的0.5mM油酸和0.5mM棕榈酸溶液中2分钟,然后倾析。然后通过碳分析分析残留的捕收剂浓度。用油酸作为捕收剂,吸附等温线在大致双层覆盖时表现出平台,与其他方法的结果一致(Marinakis&Shergold 1985,Bahr等1968)。萤石上吸附棕榈酸类物质时,吸收量比油酸盐的吸收量大得多。发现棕榈酸酯物质的吸收作为残留棕榈酸酯浓度的函数的线性图是直线(Bunge 1993),发现棕榈酸酯物质的吸收作为棕榈酸酯残余浓度的函数的直线图(Bunge 1993),其可以简单地表示为Gamma;= 4.4times;10 5 C,其中Gamma;是吸收密度,C是摩尔每升。例如,在0.4mM的残余浓度下,棕榈酸酯物质的摄取相捕收剂的大量吸收看起来是在反应的短时间内带负电的棕榈酸颗粒在带正电荷的萤石表面上的异相凝聚。这通常与前述的zeta;电位测量结果一致。
3.5萤石上的棕榈酸酯类和接触角
使用捕泡法测定不同Ca2 浓度下恒定棕榈酸盐浓度(5times;10 -7M)下pH值对萤石抛光部分接触角的影响。将气泡置于倒置的矿物标本上,用测角仪测量角度。在每种情况下,在进行测量之前,首先将含有标称浓度的Ca的溶液与棕榈酸盐在所需pH下平衡10分钟。从图6中给出的曲线可以看出,棕榈酸酯存在时的接触角在约pH在3和10之间是明显的。进行一系列实验而没有添加钙离子,产生萤石上的最大接触角(在约pH= 7下)。当存在额外的钙时,图6中给出的接触角对pH曲线清楚地显示出两个不同的峰。 在该图中,箭头标记在1mM和10mM Ca溶液中棕榈酸钙的沉淀边缘。
随着pH增加到3以上,接触角增加,在CaPa2达到沉淀边缘的pH值之前达到最大值。接触角的增加必须是通过吸附棕榈酸根离子和将HPa颗粒杂凝聚到表面上而在表面上涂覆HPa而产生的。
图6. pH对5x10-7M棕榈酸盐溶液中萤石接触角的影响,添加或不添加钙离子。 箭头表示HPa / CaPa2稳定区域的边界
在pH6左右接触角的急剧下降似乎与HPa向CaPa2的转化有关。形成的CaPa2颗粒明显不会附着在倒萤石表面。随着pH升高,棕榈酸离子会化学吸附到矿物上并反应形成表面沉淀。在pH=10左右时,由于萤石表面自身带正电荷较少,棕榈酸酯吸收停止,并且磷灰石再次变为亲水性,通过接触角减小表示出来,在接触角行为中可以看到的双峰类似于经常在氧化物矿物油酸浮选出现的现象(M.C.Fuerstenau和Palmer 1976),他们认为氧化物矿物油酸浮选这是由低pH下的物理吸附和高pH下的化学吸附产生的。
3.6用棕榈酸盐捕收剂浮选萤石
为了确定适合于进一步实验的捕收剂浓度,因此确定了捕收剂在pH 为4,7和9下浮选回收率的影响。一般来说,非常低量的棕榈酸酯足以完成萤石的浮选。在pH7时,用5times;10-7M棕榈酸酯获得了萤石的完全回收,因此所有随后的浮选试验都是在该捕收剂添加量的情况下进行的[与接触角研究中使用的相同]。浮选研究的主要重点是调查添加钙离子和pH值对萤石浮选行为的影响。
在第一组实验中,萤石样品用选定浓度的硝酸钙溶液适度搅拌平衡10分钟。除了Ca 2 的最高添加量之外,所有实验均通过添加KNO3以0.01M的离子强度进行。在从保持所需pH的0.1mM储备溶液(pH 11)中缓慢加入适量捕收剂之后,将浆液再搅拌10分钟,然后转移至Hallimond管并用氮气漂浮5分钟。图7给出了显示在四种不同硝酸钙添加水平下萤石的回收率与pH的关系的曲线。该图显示,通过该程序,添加的Ca对微酸性体系中的浮选回收几乎没有影响,而在较高的pH下具有显着的影响。在较低的Ca添加量下,完全浮选发生的整个pH范围要大得多,即用1mM Ca调节至约pH为8-9和用0.1mM Ca调节pH9-10。添加0.01M和0.1M钙时,浮选在HPa / CaPa2边界处是最
全文共8166字,剩余内容已隐藏,支付完成后下载完整资料

英语原文共 6 页,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[10976],资料为PDF文档或Word文档,PDF文档可免费转换为Word


