
英语原文共 28 页,剩余内容已隐藏,支付完成后下载完整资料
生物材料纳米结构的力学性能
摘要
天然生物材料如骨骼,牙齿和珍珠母是蛋白质和矿物质的纳米复合材料,具有优异的强度。自然用像人类的皮肤一样柔软的蛋白质,和像教室的粉笔一样脆弱的矿物质,制造出了如此坚硬而坚韧的材料,这真是一个奇迹。大自然的秘密是什么?我们能从中学到如何在实验室中生产出仿生材料吗?这些问题促使我们研究蛋白质—矿物纳米复合材料结构的力学性能。发现大纵横比和交错排列的矿物质血小板是使得生物材料拥有较大刚度的关键因素。生物纳米结构的张力剪切链(TSC)模型揭示了生物材料的强度取决于优化矿物晶体的拉伸强度。随着矿物晶体的尺寸缩小到纳米尺度,他们对强度接近原子键理论强度的缺陷变得不敏感。由于矿物晶体拉伸强度的优化,从而使得生物材料在蛋白质剪切变形中消耗大量的断裂能,并因此增强生物复合材料的断裂韧性。我们推导出蛋白质—矿物纳米结构的粘弹性性质,这种黏弹性性质表明生物复合材料的韧性可以被蛋白质的粘弹性进一步增强。
关键词:A.断裂机理; A.加强和机制; B.生物材料; B.不均匀的材料; B.粘弹性材料
1.介绍
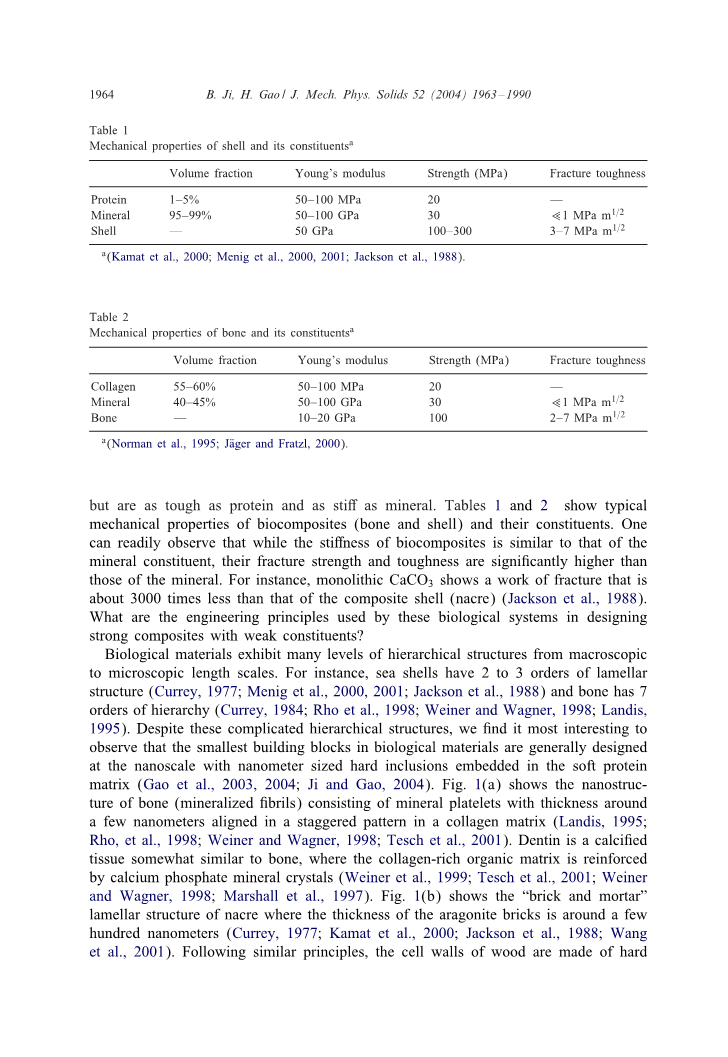
表1
壳及其组分的力学性能
体积分数 杨氏模量 强度(MPa) 断裂韧性
蛋白 1-5% 50-100MPa 20 -
矿物 95-99% 50-100GPa 30 lt;lt;1MPa m1 / 2
贝壳 - 50GPa 100-300 3-7MPa m1 / 2
表2
骨骼及其组分的力学性能
体积分数 杨氏模量 强度(MPa) 断裂韧性
胶原 55-60% 50-100 MPa 20 -
矿物 40-45% 50-100 GPa 30 lt;lt;1 MPa m1 / 2
骨骼 - 10-20 GPa 100 2-7 MPa m1 / 2
自然进化已经在动物的内外骨骼系统中产生了坚硬而坚韧的材料。骨骼,牙齿,贝壳和鹿茸是蛋白质和矿物质的复合物,但是和蛋白质一样强硬,和矿物一样坚硬。表1和2显示了生物复合材料(骨和壳)及其成分的独特力学性能。人们可以很容易地观察到,虽然生物复合材料的刚性与矿物成分相似,但它们的断裂强度和断裂韧性都远高于矿物。例如,单独的CaCO3显示的断裂功比复合壳(珍珠层)小约3000倍(Jackson等,1988)。生物系统在用弱的成分设计出具有很高的断裂强度和断裂韧性的复合材料时使用的工程原理是什么?
生物材料展现出从宏观到微观尺度的许多层次结构。例如,海贝壳具有2-3层的层状结构(Currey,1977; Menig等人,2000,2001; Jackson等人,1988),而骨骼具有7个层次结构(Currey,1984; Rho et al。 ,1998; Weiner和Wagner,1998; Landis,1995)。尽管有这些复杂的层次结构,但我们最感兴趣的是观察到生物材料中最小的构建块通常设计在纳米尺度,纳米尺寸的硬包裹体嵌入软蛋白基质中(Gao等,2003,2004; Ji and图1(a)显示了在胶原基质中交错排列的几纳米厚度的矿物薄片组成的骨骼(矿化Mbrils)的纳米结构(Landis,1995; Rho等, 1998; Weiner和Wagner,1998; Tesch等,2001)。牙本质是一种与骨骼有点相似的钙化组织,其中富含胶原蛋白的有机基质被磷酸钙矿物晶体增强(Weiner等,1999; Tesch等,2001; Weiner和Wagner,1998; Marshall等, 1997)。图1(b)显示了珍珠层的厚度为几百纳米的霰石块的“砖和灰浆”层状结构(Currey,1977; Kamat等,2000; Jackson等, 1988; Wang等人,2001)。
B. Ji,H.Hao / J.Mech。物理学。 Solids 52(2004)1963-1990 1965
图1.生物材料的纳米结构。 (a)在皮质骨中,板状矿物晶体相互堆叠并形成胶原分子的矿化胶原纤维。矿物晶体的厚度只有几纳米(Landis,1995)。这些条纹显示结构的长度尺度。 (b)在珍珠层中,矿物质小片完全互锁,以形成彼此交错堆叠的片材。矿物薄片的厚度约为几百纳米(Currey,1977; Jackson等,1988)。
遵循类似的原则,木材的细胞壁是由坚硬的细胞膜纤维嵌入软半纤维素木质素基质中组成的。以前的研究人员试图通过各种理论观点来解释生物复合材料高韧性的力学性能原理,包括它们的层次结构(Menig等人,2000,2001; Kamat等人,2000; Kessler等人,1996),蛋白质能消耗断裂能的力学性能(Smith et al。,1999),蛋白质 - 矿物界面粗糙度(Wang et al。,2001)和裂纹处应力集中的降低(Okumura and de Gennes,2001)。但是关于韧性机理和其他力学性质是如何与生物材料的纳米结构相关的问题迄今尚未受到关注。
刚度和硬度对于骨骼类生物复合材料的支撑和保护功能非常重要。尽管蛋白质相比矿物质软约3个数量级,但表1和2表明,蛋白质的存在并不显着降低生物复合材料的刚度。事实上,生物复合材料的弹性模量接近Voigt模型定义的上限。对于蛋白质 - 矿物质复合体系而言,由于矿物质和蛋白质之间的刚度差异,对刚度在上限(Voigt)和下限(Reuss)之间的范围限制可能非常大。生物材料是如何达到复合材料刚度的上限的呢?
生物复合材料的很高的强度是如何实现的?由于蛋白质基质非常软且几乎没有维持外部载荷的能力,因此必须假定硬质矿物质承载了作用于复合材料上的大部分载荷。然而,脆弱的矿物和教室的粉笔一样脆弱。矿物质成分如何在承受大应力的情况下没有发生脆性断裂?生物材料如何优化矿物晶体的强度,从而允许大量的变形能量被吸收和消散在蛋白质基质中?
作为生物材料的有机成分,蛋白质被认为在实现和保持大的韧性方面发挥重要作用。定性地说,蛋白质基质的行为就像是围绕矿物质板的软包装,并保护它们免受外部载荷引起的最大应力,并使应力分布均匀到这个复合材料。一个重要的线索是,动物的内骨骼含有比海贝壳更高的蛋白质含量。例如,骨骼中蛋白质的体积分数约为50%(JKager和Fratzl,2000),但在珍珠层中只有5%(Jackson等,1988)。这种差异可能归揭示了一个事实,那就是动物的内骨骼比海贝壳的外骨骼预计会经历更严重的动载荷和更大的生命变形。此外,蛋白质可以通过其固有的粘弹性性质(Lakes,2001; Sasaki等,1993)及其分层和粘附分子结构(Smith等,1999; Thompson等,1993)更有效地消散动态断裂能。我们如何模拟蛋白质的力学性质及其对生物复合材料性能的影响?
预计生物材料的刚度,硬度,强度和韧性的力学理论将在未来几十年中发展仿生多功能和分层材料中发挥重要作用。本文是这一盛大尝试的初步成果。在本文的第2节,我们将讨论有关生物材料纳米结构的实验研究,介绍了生物复合材料的纳米结构的张力剪切链模型。在第3节中,张力剪切链模型用于研究生物复合材料的弹性性质。在第4节中将会发展一种生物复合材料的粘弹性拉伸 - 剪切链模型。第5节讨论了纳米尺寸矿物晶体的断裂强度。在第6节中分析了生物复合材料的断裂能。第7节从粘弹性耗散,裂纹附近的应力屏蔽和损伤传感的角度阐述了蛋白质对于生物复合材料韧性的作用。我们在第8节对这篇文章进行总结
2.生物纳米结构模型
生物材料是分层结构的,其性质取决于它们在各个层次上的结构(Weiner和Wagner,1998)。最基本的层次结构发生在纳米尺度上,并且涉及到海贝壳中交错的文石砖和在骨骨骼中的矿化纤维。纳米结构会在生物材料的整体力学性能中起非常重要的作用。在这里,我们描述了一些相关的实验研究和生物材料的纳米结构的理论模型,为随后讨论生物材料的高强度,强度和韧性机理的阶段做准备。以前的研究(Jackson等,1988; Currey,1977; Menig等,2000,2001; Kamat等,2000; Wang等,2001)已经显示有一个海贝壳纳米结构的良好的组织,以交错砖块(矿物薄片)的形式粘在蛋白质层。矿物薄片的长度范围通常在100-500nm的范围内。骨和牙质具有更复杂的层次结构,并且它们的纳米结构可以被描述为嵌入在胶原基质中的交错的矿物薄片(羟基磷灰石)。骨骼和牙质中的矿物晶体的最小尺寸在几纳米左右。高压电子显微镜(HVEM)和小角度X射线散射法(SAXS)等现代实验技术的发展使研究材料从埃到纳米的内部结构成为可能。最近十年来,通过Fratzl及其同事的SAXS工作(Fratzl等,1991,1992,1996a,b,1997; Rinnerthaler等,1999 ; Paris等,2000; Tesch等,2001; Roschger等,2001)以及Landis和同事的HVEM工作(Landis等人,1993; Landis,1995; Landis和Hodgens,1996)在骨骼和牙本质的纳米结构方面取得了显着进展。X射线散射和HVEM实验揭示了骨骼和牙本质的基本结构晶体的尺寸和几何形状(Fratzl等,1997; Paris等,2000; Tesch等,2001; Landis等, ,1993; Landis,1995; Landis和Hodgens,1996)。发现矿物晶体的形状非常不等轴(薄片)。对于骨骼,牙本质(3nm厚和长达100nm长的薄片)和牙釉质(颗粒15-20nm厚,1000nm长;参见例如Warshawsky,1989)的不等轴比珍珠层更大(薄片200-500nm厚5-8mu;m长;参见例如Wang等,2001; Kamat等,2000)。矿物晶体的尺寸和几何形状被认为在生物材料的力学性能中起重要作用。
在单个矿物纤维的水平上,生物材料的力学性能将取决于矿物晶体在纤维中的精确排列(Weiner和Wagner,1998; Rho等,1998; JKager和Fratzl,2000; Landis等, ,1993; Landis,1995; Landis和Hodgens,1996)。 Fratzl及其合作者(Fratzl等,1992,1996a,b,1997; Rinnerthaler等,1999; Paris等, 2000; Tesch等,2001)使用SAXS和Landis及其同事(Landis等,1993; Landis,1995; Landis和Hodgens,1996)使用HVEM层析成像研究了骨骼和牙本质蛋白质基质中矿物晶体的趋向和组织。由于矿物和有机基质之间的大电子密度差导致强烈的SAXS信号,使得SAXS非常适合确定胶原基质中矿物晶体的大小,形状和趋向。已知在骨骼的纳米结构中,矿物晶体具有大的纵横比并且沿着更好的定向胶原纤维排列平行于骨骼的纵轴的(Bundy,1985)。非静水力学热力学预测,晶体生长与主应力方向平行,并且表明生物组织中的矿物趋向可能被功能负荷(Williams,1989)影响。基于对骨骼和牙齿的HVEM和X射线观察,JKager和Fratzl(2000)和Landis(1995)提出了矿物晶体以交错模式在蛋白质基质排列的模型。矿物薄片交错排列与胶原蛋白纤维空隙的分布一致(Hodge and Petruska,1963)。这些研究表明,矿物晶体排列对于骨骼的强度和断裂非常重要。例如,成骨不全症是由蛋白质中矿物晶体不正常排列引起的严重骨骼疾病(Landis,1995)。
图2.生物复合材料的模型。 (a)完全交错的嵌入蛋白质基质中的矿物包裹体。 (b)生物复合材料的拉伸剪切链模型,其中消除蛋白质的拉伸区域以加强复合材料结构内的载荷传递。 (c)矿物晶体的自由体图。
矿物薄片的更好的趋向排列使得生物复合材料固有地具有各向异性。各向异性特性有助于生物更好的适应自然演化中的各种环境下的负荷。骨骼在两个正常方向上可以达到1.7-2.1的各向异性比率(Hasegawa等,1994; Turner和Burr,1997; Turner等,1995; Pidaparti等,1996)。根据海贝壳的层状宏观和微观结构够可以发现它具有很强的各向异性力学性能(Currey,1977)。基于JKager和Fratzl(2000)的先前对骨骼纤维交错排列的研究工作,Gao等人(2003)提出了一个一维复合模型来研究骨骼,牙本质和贝壳的纳米尺度下的有效刚度,如图2(a)所示。矿物晶体具有较大的纵横比并且比软蛋白基质硬得多,假定矿物晶体末端附近的蛋白质基质中的拉伸区域不承受力学载荷。载荷很大程度上是被矿物血小板长边之间的蛋白质高剪切区域转移了。因此,图2(a)的复合材料模型可以简化为图2(b),其中柔性相的拉伸区域从复合结构中消除了。在施加的拉应力下,矿物薄片承载大部分拉伸负荷,而蛋白质基质通过剪切将矿物晶体间的负荷转移。复合材料中的载荷传递路径简化为矿物元
全文共7426字,剩余内容已隐藏,支付完成后下载完整资料
资料编号:[11386],资料为PDF文档或Word文档,PDF文档可免费转换为Word


