透明质酸结合氧化石墨烯进行靶向药物输送外文翻译资料
2022-09-30 11:29:23

英语原文共 11 页,剩余内容已隐藏,支付完成后下载完整资料
透明质酸结合氧化石墨烯进行靶向药物输送
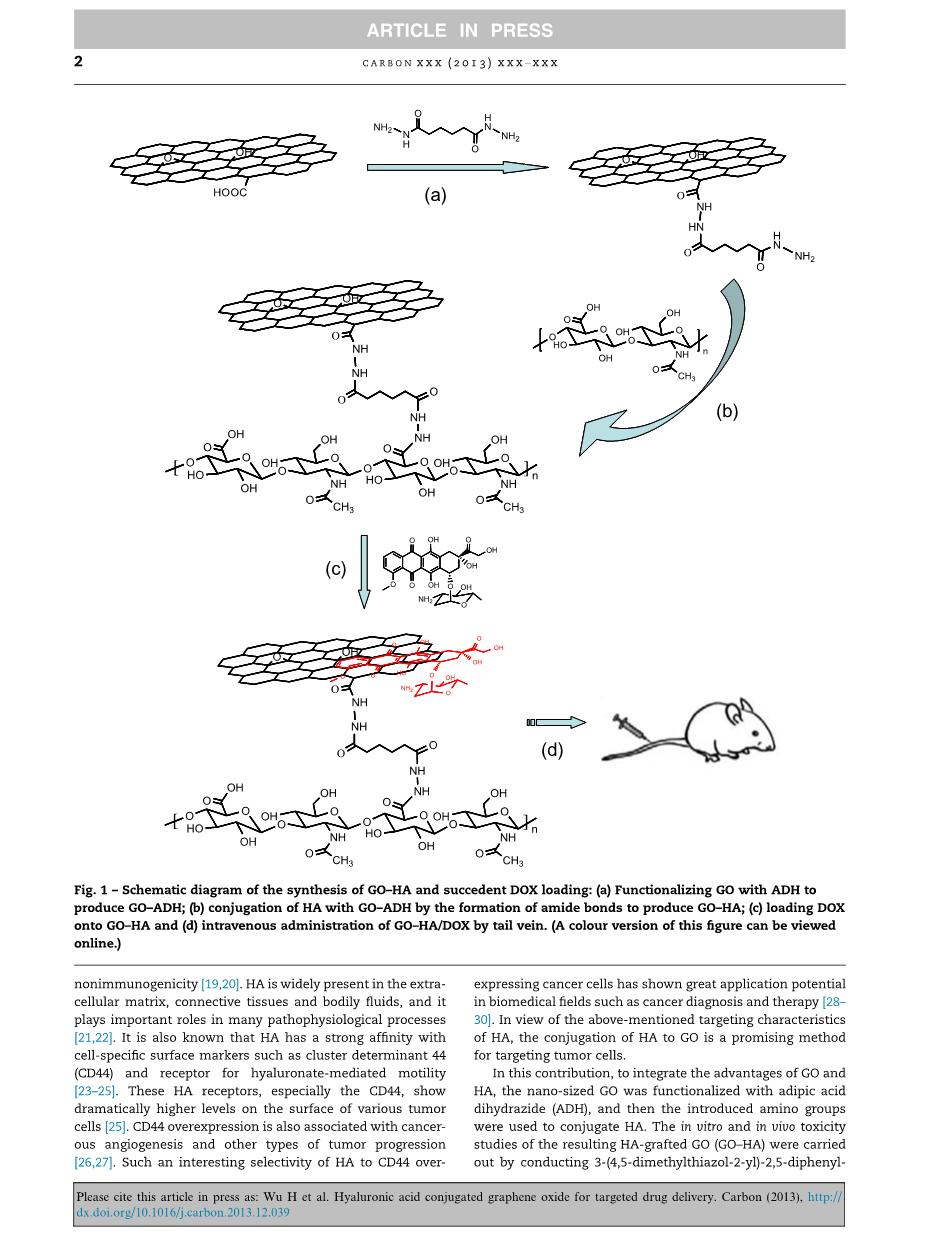
纳米级氧化石墨烯与己二酸二酰肼结合功能化后引入官能团氨基,然后透明质酸(HA)借助酰胺结合与氧化石墨烯(GO)形成共价结合。结果GO-HA溶血活性可以忽略不计,而且对海拉和L929细胞的毒性很低,它可以通过受体介导的内吞作用有效地吸收肿瘤细胞。组织学、血液学和生化分析结果显示GO-HA在小鼠体内的含量为10mg/kg、曝光时间为10天的情况下没有明显的毒性。阿霉素(DOX)可以有效地加载到GO-HA上,并且由此产生的GO-HA /DOX对海拉细胞展现了明显的的细胞毒性。GO-HA的体内药物输送过程可以通过静脉注射GO-HA /DOX后的肿瘤在小鼠体内生长来进行演示。结果表明,GO-HA可以有效地把阿霉素传递到肿瘤细胞中并且可以抑制肿瘤的生长。
1.简介
石墨烯作为一个二维的sp2碳网络隔离材料,第一次出现在2004年时,由于其非凡的化学、光学、电和机械性能和在纳米电子设备、透明导体和复合材料上潜在的应用,石墨烯已经吸引了巨大注意。最近,石墨烯也用于生物医学领域,如药物/基因传递、生物传感、分子成像和癌症治疗[4]。特别是,对药物衍生来说,功能化氧化石墨烯及其衍生物已成为有前途的材料。具有独特的特性,如能够简单合成,在水中以及生理环境中的高散性、良好的生物相容性和轻松可调的表面功能化,这对于生物应用非常有利。重要的是,它的双面都可以用于加载药物,所以它有非常高的载药量。此外,氧化石墨烯和药物之间的动态结合作用(例如,p-p叠加,疏水性,氢键和静电相互作用)能够控制响应外界刺激(如pH值、温度、化学物质和电场)。因此,控制药物释放可以通过不同的路线。所有这些有利的属性让氧化石墨烯比其他含碳质纳米材料更加有效的作为药物载体在体外和体内生物应用。
作为一种由N-乙酰基-D-葡萄糖胺和D-葡萄糖酸交替组成的天然多糖,透明质酸(HA)具有独特而优秀的物理化学属性,如生物降解性、生物相容性和无致免疫性。HA广泛存在于细胞外基质,结缔组织和体液中,在许多病理生理过程中扮演着重要的角色。众所周知HA对细胞表面分子有很强的亲和力,如CD44和受体RHAMM。这些受体,尤其是CD44,高水平的显示了表面的各种肿瘤细胞。CD44也能高度表达与癌症有关的血管生成和其他类型的肿瘤进展情况。这样一个有趣的选
择性有关HA的受体CD44发现癌细胞已经在生物医学等领域显示出巨大的应用潜力,例如进行癌症诊断和治疗。针对上述HA的目标特征,HA与GO结合的话,是一个针对肿瘤细胞有前途的方法。
在这个设计中,去整合氧化石墨烯和透明质酸的优点,纳米级氧化石墨烯和已二酸二酰肼(ADH)结合而进行功能化,然后引进氨基,进而和HA结合。GO-HA的体外和体内毒性研究结果通过四甲基偶氮唑盐(MTT)传到试验,血液和血清的生物化学测量,以及组织学评估而得出。盐酸阿霉素(DOX/EHCl),一种亲水性药物,可以用一种可控制的方法加载到功能化氧化石墨烯上。对GO-HA载阿霉素到海拉细胞表面上的CD44进行体外选择性靶向和细胞毒性效应检查。此外,对海拉肿瘤小鼠静脉注射GO-HA/DOX的化学疗法影响也进行了研究。
培养在常规生长介质组成的罗斯威尔公园纪念研究所介质(RPMI)1640用10%胎牛血清,在37℃、5%的二氧化碳气氛下。细胞用乙二胺四乙酸(EDTA)(0.25%)溶解处理后,还是照常收获。
2.实验
2.1 化学原料
已二酸二酰肼(ADH)(P98%)是由TCI提供。透明质酸从上海浩然生物技术有限公司获得。盐酸阿霉素从北京华丰联合科技有限公司获得。其他的化学物质和试剂购自国药控股的化学物质和试剂公司,电阻率高于18MX 厘米的去离子水用于整个实验。氧化石墨烯用修改后的赫莫兹方法制取,用天然石墨粉做原材料。
2.2 GO-HA的合成
GO(50mg)分散在蒸馏水(50ml)中,然后加入250mgEDC和750mgNHS来向GO上引入羧酸基团。520gADH加入GO溶液中,接着搅拌反应24h。产品GO-ADH离心分离,并且用蒸馏水反复冲洗。透明质酸(15mg)、EDC(38mg)、NHS(113mg)溶解在磷酸缓冲溶液(PBS,PH=5.6,15ml)中,然后加入上述的GO-ADH,混合后室温下搅拌反应24h。反应结束后通过离心来分离产品GO-HA,并且用蒸馏水反复冲洗,然后分散在PBS(PH=7.4)溶液中。
2.3 特性表征
透射电子显微镜(TEM)图像是在日本电子光学实验室中的JEM-2100高分辨率传输电子显微镜上获得的。形态分析用维异科多状态原子力显微镜(AFM)。用溴化钾小球,将傅里叶变换红外光谱记录在一个 Nicolet Avatar 370红外光谱分光光度计上。X射线衍射(XRD)模式是使用Cu-Ka辐射(k = 0.15405 nm) (40 kV, 40mA)在一个理学最大动态密度为2000的X衍射仪上制得的。拉曼光谱是在一个超级LabRam二世共焦显微拉曼光谱仪仪器(Dilor、法国)上采集的。紫外-可见光吸收光谱是在美国贝克曼·库尔特DU 730分光光度计上得到的。
2.4 细胞培养
海拉和L929细胞株由中国科学院上海生命科学研究院生物化学和细胞学协会提供,这些细胞株培养在常规生长介质组成的罗斯威尔公园纪念研究所介质(RPMI)1640用10%胎牛血清,在37℃、5%的二氧化碳气氛下,细胞用乙二胺四乙酸(EDTA)(0.25%)溶解处理后,还是照常收获。
2.5 体外细胞毒性和溶血反应试验
细胞毒性:海拉和L929细胞株被用来评估GO和GO-HA的体外细胞毒性。这些细胞放在96孔的细胞培养皿上,浓度为每孔中1.104个细胞,5%二氧化碳下、37℃下培养24小时。然后让这些细胞暴露在一定浓度原料中,进一步培养12或者24h。最后,细胞生存能力用MTT法进行评估。细胞毒性可表示为活细胞与未处理细胞的百分比。
溶血试验:由上海血液中心提供的人类红细胞对乙二胺四乙酸(EDTA)非常亲和。体外溶血反应试验可以通过文献资料法实现。测试材料的密度为:50、100、200、300和400mu;g/ml。
2.6 体内毒性研究
从中国科学院上海实验动物中心获得的健康雄性昆明小鼠(体重20 g),
所有动物的操作都按照动物保护和使用委员会的制度来进行。GO-HA分散在生理盐水(0.2毫升)中,并且按照10mg/kg的剂量通过尾巴静脉血管给昆明小鼠(每组3只小鼠)进行注射。只注射生理盐水的那组昆明小鼠(n = 3)被选为控制组。组织学和血液学研究:血液样品和组织在注射后4小时和10天后从小鼠体内获得。用一对组织钳在眼眶里面快速移动眼球来收集血液。肾脏功能的两个指标(肌酐和血尿素氮)和三个重要肝脏功能指标(丙氨酸转氨酶、天冬氨酸转氨酶、总胆红素)测定。为制备血涂片,将一滴血放置在幻灯片一端并且沿着幻灯片的长度分散到另一个幻灯片。幻灯片经空气干燥,之后将血液染上苏木精伊红来区分每一组细胞。在完成采血后,老鼠被牺牲了。心脏,肝脏,脾脏,肺和肾脏被移除安装在4%甲醛中,然后脱水和嵌入在石蜡中。用切片机切取5毫米横部分,并且用苏木精伊红染色进行组织学分析。
2.7 发光成像
共焦荧光成像用徕卡TCS SP5 II激光扫描共焦显微镜63·oilimmersion物镜来完成。细胞被播种在盖玻片上,用30mu;g/ml GO-HA -DOX/和GO-DOXf孵化 3 h。细胞用PBS溶液洗3次,在测量前用DAPI溶解。
2.8 载药量、释放和细胞毒性
在GO-HA上负载阿霉素是由混合盐酸阿霉素和原料(5毫克)在PBS缓冲液(pH = 7.4,10毫升)和一个特定的药物浓度下皮光反应20小时完成的。产品GO-HA /DOX通过离心收集,用PBS反复洗净去除多余的药物。阿霉素的负载率在490纳米下用紫外可见光谱估计。研究阿霉素在GO–HA, GO–HA/DOX的释放行为,密封在透析膜中,并悬浮在PBS缓冲(2.0毫升,pH值为7.4,2.0和5.2)中。透析袋在相同的pH值、37度、震动下孵化在PBS缓冲(8.0毫升)中。通过紫外可见分光光度计(490纳米)来测定阿霉素在不同的时间下的量。每个实验重复了三次。自由阿霉素和GO-HA /DOX对海拉的细胞毒性用MTT检测。这个试验过程类似于GO-HA的细胞毒性试验。
2.9 体内肿瘤治疗
海拉肿瘤模型是通过皮下注入5·106细胞RPMI 1640(0.2毫升)进入裸体小鼠左外侧的腹壁而制作的。当肿瘤大小达到100mm3左右治疗再开始。老鼠被分为三组,每个实验组包括3只小鼠。老鼠用(a)生理盐水(200mu;L),(b)GO-HA(200mu;L,10mg/kg),(c)GO-HA /DOX(200mu;L 6mg/kg的阿霉素,与b组相同数量的GO-HA )通过尾静脉每三天注射一次。肿瘤体积和体重几天检测一次。肿瘤体积计算使用以下公式:肿瘤体积=(肿瘤长度)times;(肿瘤宽度)sup2;/2。相对肿瘤体积计算V / V0(V0是治疗开始时肿瘤体积)。
2.10 统计分析
统计分析使用未配对学生t分布来完成。这些数据意味着plusmn;标准偏差。AP值小于0.05被认为是统计有很重要的意义。
3. 结果与讨论
3.1 GO-HA的合成与表征
水溶性氧化石墨烯是用氧化的石墨根据改进的Hummers法、接着用声波降解法处理来进行制备的。制得的氧化石墨烯可在纯水中稳定的存在一个月并且不会发生结块现象。透射电子显微镜图(TEM。图a)和原子力显微镜图(AFM。图b)为准备好的氧化石墨烯提供形态信息。纳米片有0.8-1.3nm的厚度,暗示氧化石墨烯是石墨上的单层完整结构。氧化石墨烯的实际厚度比单层石墨的理论厚度大是因为共价键O-X-O的存在。氧化石墨烯的结构展示了良好的分离,它们的横向宽度发生了60-500nm的变化,并且百分之八十的氧化石墨烯的结构小于300nm。
化石墨烯的红外光谱谱图(图e)揭示了-OH(3380cm-1),C=O(1725 cm-1),C=C(1622 cm-1),C-O(1060 cm-1)的存在。合成的氧化石墨烯进一步用X射线衍射来研究。如图f所示,一个强烈的峰出现在11.3(d = 0.78nm),通常出现在氧化石墨烯样品的x射线衍射模式里面。这个峰值由于在X射线样品采集准备过程中氧化石墨烯模拟方式的峰值堆叠形成的。石墨的特征衍射峰值在26.5处消失是因为石墨的完全氧化。氧化石墨烯的拉曼光谱(图g)展示了出现在1333和1592的两个强峰,分别标记为D和G。D和G处氧化石墨烯的比值大约为1.2,比原先准备好的氧化石墨烯(0.79)要高。要显著增加氧化石墨烯中D和G的比值相对于石墨和石墨氧化物来说,建议在单层石墨上引进高层次的障碍,并在氧化和随后的剥落中,减少平面sp2结构域。与石墨氧化物相比,氧化石墨烯的2D结构在2700-2650 cm-1之间移动。2D结构是区界声子的第二等级结构。2D峰值的移动取决于单层石墨的数量。单层石墨展示单层2D结构峰值在2700 cm-1的下面,同时双分子层或者多分子层有宽广的和高速的2D峰值在2700 cm-1附近或者大于它。氧化石墨烯的拉曼光谱证明了2D峰值低于2700 cm-1,说明了氧化石墨烯的结构是单分子晶体结构。
透射电子显微图像(a),原子力显微图像(b)和高度直方图(c),原子力粒度分布图像(d)、傅立叶变换红外光谱图(e),x射线衍射模式(f)和氧化石墨烯的拉曼光谱(g)。原始石墨粉的x射线衍射模式(f)。
GO-ADH(a)、GO-HA(b)、HA(c)的傅里叶红外光谱图(A),GO-HA的原子力显微图和宽度直方图(B)
为了引入氨基去进一步移植透明质酸,事先准备好的氧化石墨烯首次通过碳化二亚胺耦合结合ADH。图3A是已经获得的GO-ADH的红外光谱图,它揭示了消失的C=O拉伸变成了-COOH(1725 cm-1),并且由于酰胺键的出现导致在1630 cm-1处出现了一个强键。同时,使用标准的FMOC,氨基在GO=ADH中存在的量有5.9times;10-5mol/g,所以其中共轭ADH占1.0%。然后,GO-ADH中的主要氨基才可以通过酰胺键与HA发生反应。GO-HA的红外光谱图见图3A。一些新的吸光度特征出现在1627cm-1(酰胺键),1405 cm-1 (羧化物对称拉伸),1155 cm-1 (骨骼缩醛价带)和1045 cm-1 (C-O键),才确认HA与GO成功的结合在一起了。HA在GO-HA中的量通过热重量法来估算。原始氧化石墨烯的热谱图显示在120℃下重量会损失10%,这与它吸附水分子的多少有关。在120-160℃范围内出现重大损失(31%)是由于含水集团的分解。通过GO-HA的热重量曲线可以看出在120-220℃之间,大概有14%的重量损失,这是由于GO中剩下的含氧集团小时而导致的。49%的显著重量损失相当于GO整体剥落引入HA。根据GO和GO-HA的热重量数据分析,嫁接HA段的重量百分比大概是49%,忽略结合ADH的数量。图3B显示了GO-HA的原子力显微图。GO-HA分散
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[150186],资料为PDF文档或Word文档,PDF文档可免费转换为Word
课题毕业论文、开题报告、任务书、外文翻译、程序设计、图纸设计等资料可联系客服协助查找。



